Hoá học 9 Bài 44: Rượu etylic
Khi lên men gạo, sắn, ngô (đã nấu chín) hoặc quả nho, quả táo... người ta thu được rượu etylic. Vậy rượu etylic có công thức cấu tạo như thế nào? Nó có những tính chất và ứng dụng ra sao? Các em cùng tìm hiểu qua bài học này.
Mục lục nội dung

1. Tóm tắt lý thuyết
Công thức phân tử: C2H5OH
Phân tử khối: 46 g/mol
1.1. Tính chất vật lý
a) Khái niệm
- Rượu Etylic là chất lỏng không màu, nhẹ hơn nước.
- Sôi ở 78,3oC.
- Nhẹ hơn nước và tan vô hạn trong nước. Rượu Etylic hòa tan được nhiều chất như iot, benzen…
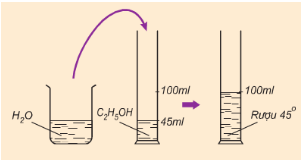
b) Độ rượu là gì? Cách tính độ rượu.
Độ rượu là số ml rượu Etylic nguyên chất có trong 100ml hỗn hợp rượu etylic với nước.
1.2. Cấu tạo phân tử
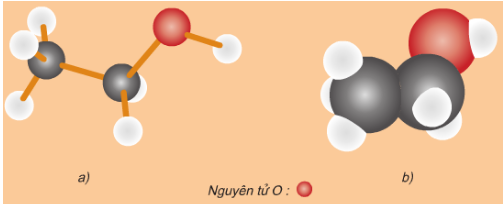
a) Dạng rỗng; b) Dạng đặc
Rượu Etylic có công thức cấu tạo thu gọn là CH3 – CH2 – OH
Trong phân tử rượu Etylic có một nguyên tử Hidro không liên kết với nguyên tử Cacbon mà liên kết với nguyên tử Oxi tạo ra nhóm – OH. Chính nhóm – OH này làm cho rượu có tính chất hóa học đặc trưng.
1.3. Tính chất hóa học
a) Rượu etylic có cháy không?
Rượu etylic tác dụng với oxi khi đun nóng theo phương trình C2H6O(l) + 3O2(k) → 2CO2(k) + 3H2O(h)
b) Rượu etylic có tác dụng với Natri không?
Natri phản ứng với rượu etylic giải phóng khí H2 theo phương trình 2CH3-CH2-OH + 2Na → 2CH3-CH2-ONa + H2
c) Phản ứng với axit axetic
Rượu etylic tác dụng với axit axetic tạo etyl axetat theo phản ứng
C2H5OH + CH3COOH 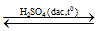 CH3COOC2H5 + H2O
CH3COOC2H5 + H2O
1.4. Ứng dụng của rượu etylic

1.5. Điều chế rượu etylic
- Phương pháp 1: Tinh bột hoặc đường \(\overset{len men}{\rightarrow}\) rượu Etylic

- Phương pháp 2: C2H4(k) + H2O(l) \(\overset{Axit}{\rightarrow}\) C2H5OH
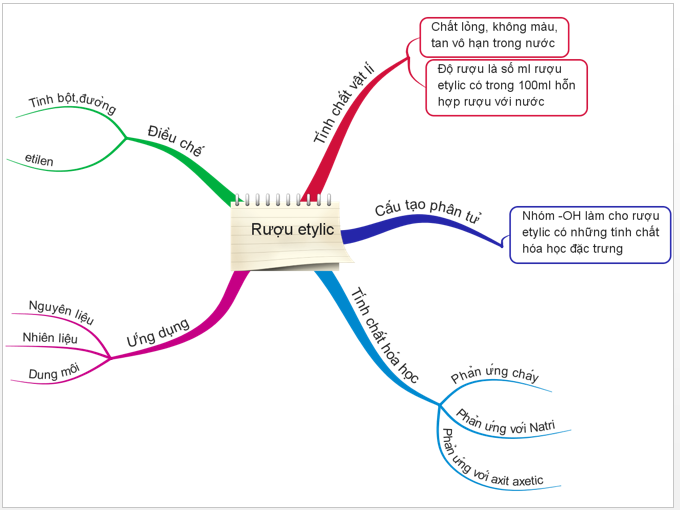
1.6. Tổng kết
2. Bài tập minh họa
2.1. Dạng 1: Hiệu suất phản ứng
Cho 11,2 lít khí etilen ( đktc) tác dụng với nước có axit sunfuric (H2SO4) làm xúc tác, thu được 9,2 gam rượu etylic. Tính hiệu suất phản ứng.
Hướng dẫn giải
Số mol khí etilen là: \({n_{{C_2}{H_4}}} = \frac{{11,2}}{{22,4}} = 0,5(mol)\)
Phương trình phản ứng: C2H4(k) + H2O(l) \(\overset{Axit}{\rightarrow}\) C2H5OH
0,5 → 0,5
Khối lượng rượu etylic thu được theo lí thuyết là: m = 0,5.46 = 23 gam
Đề bài cho khối lượng rượu etylic thu được thực tế là 9,2 gam
Hiệu suất phản ứng là: \(H = \frac{{{m_{tt}}}}{{{m_{lt}}}}.100 = \frac{{9,2}}{{23}}.100 = 40\%\)
2.2. Dạng 2: Tính độ rượu
Câu 1: Đốt cháy hoàn toàn 12 ml rượu etylic chưa rõ nồng độ. Cho toàn bộ sản phẩm vô nước vôi trong dư người ta thu được 40 gam kết tủa. Xác định độ rượu biết khối lượng riêng của Rượu etylic là 0,8 gam/ml.
Hướng dẫn giải
- Cách 1:
Ta có: \({n_{CaC{O_3}}} = \frac{{40}}{{100}} = 0,4(mol)\)
Phương trình phản ứng là:
C2H5OH + 3O2 → 2CO2 + 3H2O (1)
0,2 \(\leftarrow\) 0,4
CO2 + Ca(OH)2 → CaCO3\(\downarrow\) + H2O (2)
0,4 \(\leftarrow\) 0,4
Khối lượng của rượu etylic là: \({m_{{C_2}{H_5}OH}} = 0,2.46 = 9,2(gam)\)
Ta có: m = D.V ⇒ \(V = \frac{m}{D} = \frac{{9,2}}{{0,8}} = 11,5(ml)\)
Vậy độ rượu là: \(\frac{{11,5}}{{12}}.100 = {96^0}\)
- Cách 2:
Ta có: \({n_{CaC{O_3}}} = \frac{{40}}{{100}} = 0,4(mol)\)
Bảo toàn nguyên tố Cacbon theo sơ đồ phản ứng như sau:
C2H5OH → 2CO2 → 2CaCO3
0,2 \(\leftarrow\) 0,4
Khối lượng của rượu etylic là: \({m_{{C_2}{H_5}OH}} = 0,2.46 = 9,2(gam)\)
Ta có: m = D.V ⇒ \(V = \frac{m}{D} = \frac{{9,2}}{{0,8}} = 11,5(ml)\)
Vậy độ rượu là: \(\frac{{11,5}}{{12}}.100 = {96^0}\)
Câu 2: Cần bao nhiêu thể tích rượu nguyên chất cho vào 60 ml dung dịch rượu 400 thành rượu 600
Hướng dẫn giải
Chất tan thay đổi ,dung dịch thay đổi , nồng độ thay đổi.
Thể tích rượu nguyên chất trong dung dịch lúc đầu là:
Độ rượu = \(\frac{{{V_{ruou{\rm{ nguyen chat}}}}}}{{{V_{dd}}}}.100\) ⇒ VRượu nguyên chất = (Độ rượu.Vdd)/100 = \(\frac{{40.60}}{{100}} = 24(ml)\)
Thể tích dung dịch rượu nguyên chất sau khi pha là 24 + x (ml)
Thể tích dung dịch rượu lúc sau là: 60 + x (ml)
Thay vào công thức tính độ rượu lúc sau ta có:
\(60 = \frac{{24 + x}}{{60 + x}}.100 \Rightarrow x = 30(ml)\)
Vậy nếu ta thêm 30 ml rượu nguyên chất vào 60 ml rượu 400 thì sẽ thành rượu 600
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Trên các chai rượu đều có ghi các số, thí dụ 45o, 18o, 12o.
a) Hãy giải thích ý nghĩa của các số trên.
b) Tính số ml rượu etylic có trong 500ml chai rượu 45o.
c) Có thể pha được bao nhiêu lít rượu 25o từ 500ml rượu 45o.
Câu 2: Hòa tan m gam ancol etylic (D = 0,8 gam/ml) vào 216 ml nước (D = 1 gam/ml) tạo thành dung dịch A. Cho A tác dụng với Na dư thu được 170,24 lit (đktc) khí H2. Dung dịch A có độ rượu bằng bao nhiêu?
Câu 3: Lên men 1 lit ancol etylic 23 độ thu được giấm ăn. Biết hiệu suất lên men là 100% và khối lượng riêng của ancol etylic là 0,8 gam/ml. Khối lượng axit axetic trong giấm là bao nhiêu?
Câu 4: Biết khối lượng riêng của C2H5OH là 0,8 gam/ml, khi đó khối lượng glucozo cần để điều chế 1 lit dd rượu etylic 40º với hiệu suất 80% là bao nhiêu?
3.2. Bài tập trắc nghiệm
Câu 1: Độ rượu là:
A. số ml rượu etylic có trong 100 ml hỗn hợp rượu với nước.
B. số ml nước có trong 100 ml hỗn hợp rượu với nước.
C. số gam rượu etylic có trong 100 ml hỗn hợp rượu với nước.
D. số gam nước có trong 100 gam hỗn hợp rượu với nước.
Câu 2: Trong 100ml rượu 45o có chứa:
A. 45 ml nước và 55 ml rượu nguyên chất.
B. 45 ml rượu nguyên chất và 55 ml nước.
C. 45 gam rượu nguyên chất và 55 gam nước.
D. 45 gam nước và 55 gam rượu nguyên chất.
Câu 3: Rượu etylic là:
A. chất lỏng không màu, nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như iot, benzen,…
B. chất lỏng màu hồng , nhẹ hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như: iot, benzen,…
C. chất lỏng không màu, không tan trong nước, hòa tan được nhiều chất như: iot, benzen,…
D. chất lỏng không màu, nặng hơn nước, tan vô hạn trong nước, hòa tan được nhiều chất như: iot, benzen,…
Câu 4: Muốn điều chế 100ml rượu 65o ta dùng:
A. 100 ml nước hòa với có 65 ml rượu nguyên chất.
B. 100 ml rượu etylic nguyên chất có 65 ml nước.
C. 65 ml rượu etylic nguyên chất hòa với 35 ml nước.
D. 35 ml rượu nguyên chất với 65 ml nước.
4. Kết luận
Sau bài học cần nắm:
- Công thức phân tử, công thức cấu tạo, đặc điểm cấu tạo.
- Tính chất vật lí : Trạng thái , màu sắc, mùi vị, tính tan, khối lượng riêng, nhiệt độ sôi.
- Khái niệm độ rượu.
- Tính chất hóa học: Phản ứng với Na, với axit axetic, phản ứng cháy.
- Ứng dụng : làm nguyên liệu dung môi trong công nghiệp.
- Phương pháp điều chế ancol etylic từ tinh bột , đường hoặc từ etilen.
Tham khảo thêm
- doc Hoá học 9 Bài 45: Axit axetic
- doc Hoá học 9 Bài 46: Mối liên hệ giữa etilen, rượu etylic và axit axetic
- doc Hoá học 9 Bài 47: Chất béo
- doc Hoá học 9 Bài 48: Luyện tập Rượu etylic, axit axetic và chất béo
- doc Hoá học 9 Bài 49: Thực hành: Tính chất của rượu và axit
- doc Hoá học 9 Bài 50: Glucozơ
- doc Hoá học 9 Bài 51: Saccarozơ
- doc Hoá học 9 Bài 52: Tinh bột và xenlulozơ
- doc Hoá học 9 Bài 53: Protein
- doc Hoá học 9 Bài 54: Polime
- doc Hoá học 9 Bài 55: Thực hành: Tính chất của gluxit
- doc Hoá học 9 Bài 56: Ôn tập cuối năm



