Hoá học 9 Bài 42: Luyện tập chương 4 Hiđrocacbon - Nhiên liệu
Ở những bài học trước các em đã được tìm hiểu về Metan, Etilen, Axetilen và Benzen. Vậy giữa công thức cấu tạo với tính chất hóa học của chất có mối quan hệ như thế nào? Ứng dụng của chúng là gì? Hãy cùng nhau tìm hiểu tất cả thông qua bài giảng Luyện tập chương 4 Hiđrocacbon - Nhiên liệu.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Hệ thống kiến thức về Hiđrocacbon
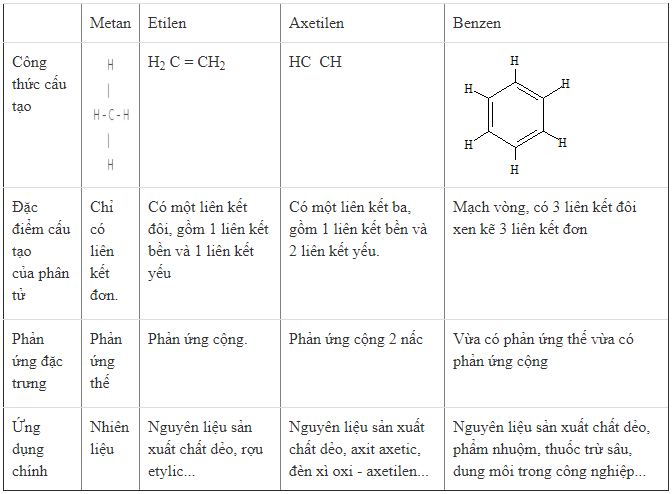
1.2. Sơ đồ tư duy tổng kết bài học
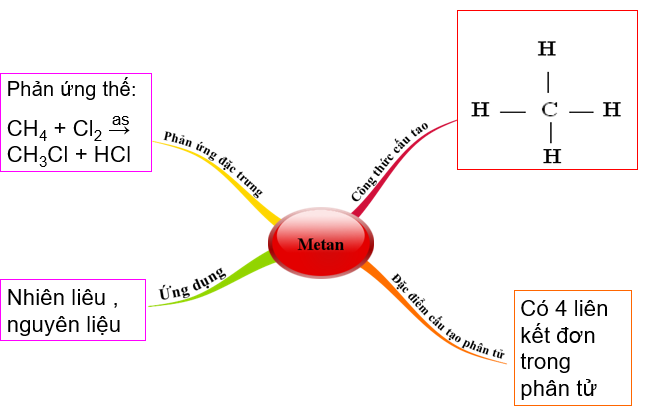
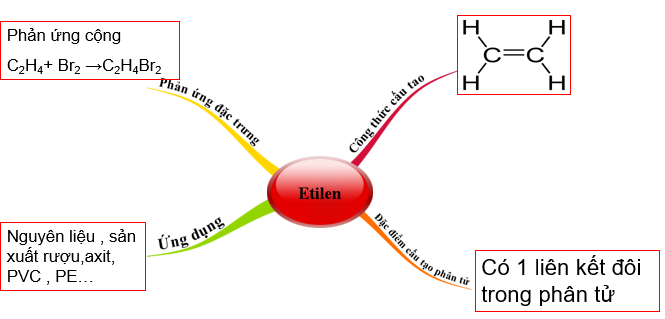
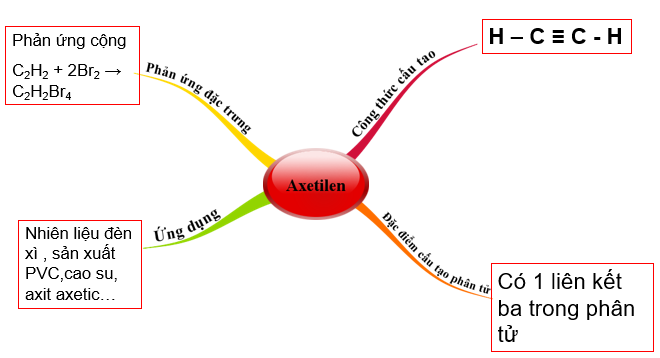
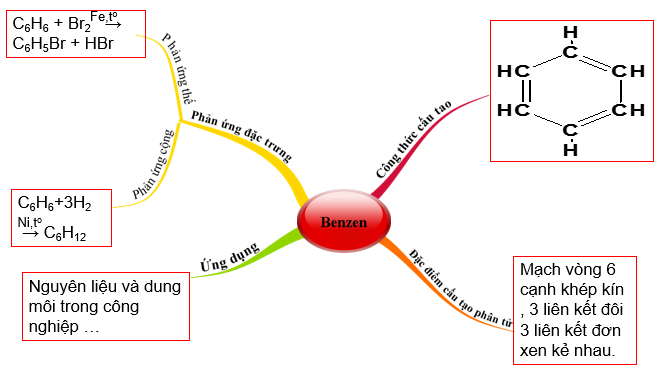
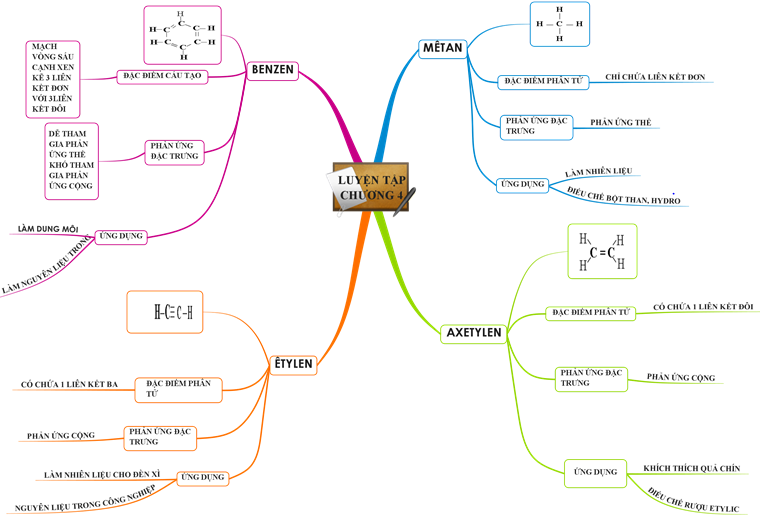
2. Bài tập minh họa
2.1. Dạng 1: Nhận biết chất khí
Có 3 bình không nhãn đựng các khí sau: CH4 , CO2, C2H4. bằng phương pháp hóa học, hãy nhận biết chúng.
Hướng dẫn giải
- Dùng dung dịch Brom nhận biết C2H2:
C2H2 + Br2 → C2H4Br2
- Dùng nước vôi trong nhận biết CO2, khí còn lại là CH4:
CO2 + Ca(OH)2 → CaCO3 + H2O
2.2. Dạng 2: Phản ứng cháy hidrocacbon
Đốt cháy hoàn toàn 6,72 lit khí C2H2.
a, Viết phương trình phản ứng xảy ra?
b, Tính khối lượng CO2 thu được.
c, Cho toàn bộ lượng CO2 thu được đi qua dung dịch Ca(OH)2 dư. Tính khối lượng chất rắn thu được?
Hướng dẫn giải
Số mol khí C2H2 tham gia phản ứng là:
Phương trình phản ứng: 2C2H2 + 5O2 .PNG)
Số mol theo phương trình: 2 mol 5 mol 4 mol 2 mol
Số mol theo đề bài: 0,3 mol → 0,6 mol
b) Khối lượng CO2 thu được là:
m CO2 = n.M = 0,6. 44 = 24,4 g
c) Khi cho CO2 đi qua dung dịch Ca(OH)2; phương trình phản ứng xảy ra là:
CO2 + Ca(OH)2 → CaCO3 + H2O
Từ phương trình ta có: nCO2 = nCaCO3 = 0,6 mol/
Khối lượng chất rắn CaCO3 thu được là: 0,6.100 = 60 gam.
2.3. Dạng 3: Xác định công thức phân tử
Hiđrocacbon A, B mạch hở có tỉ khối đối với H2 tương ứng là 22 và 13.
a) Xác định công thức phân tử và công thức cấu tạo của A, B.
b) Dẫn 5,6 lít hỗn hợp A, B có tỉ khối đối với H2 là 18,4 qua dung dịch nước brom dư sao cho phản ứng xảy ra hoàn toàn. Hãy tính khối lượng brom đã tham gia phản ứng (biết thể tích khí đo ở đktc).
Hướng dẫn giải
a) Ta có MA = 22.2 = 44 gam/mol; MB = 13.2 = 26 gam/mol
Gọi công thức của A là CxHy ⇒ 12x + y = 44 ⇒ x = 3; y = 8
Công thức của A là C3H8
- Tương tự ta có công thúc của B là C2H2
Công thức cấu tạo của B là CH≡CH
b) Gọi số mol của C2H2 có trong hỗn hợp là x → nC3H8 = 5,6/22,4 - x(mol)
Ta có:
\(\overline M = \frac{{26x + 44.(0,25 - x)}}{{0,25}} = 18,2.2 \to x = 0,1\)
Phương trình hóa học:
C2H2 + 2Br2 → C2H2Br4
Vậy mBr2 đã phản ứng là: 0,2 . 160 = 32 (gam).
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Có hai bình đựng hai chất khí là CH4, C2H4. Chỉ dùng dung dịch brom có thể phân biệt được hai chất khí trên không? Nêu cách tiến hành.
Câu 2: Đốt cháy 3 gam chất hữu cơ A, thu được 8,8 gam khí CO2 và 5,4 gam H2O
a) Trong chất hữu cơ A có những nguyên tố nào?
b) Biết phân tử khối của A nhỏ hơn 40. Tìm công thức phân tử của A.
c) Chất A có làm mất màu dung dịch brom không?
d) Viết phương trình hóa học của A với clo khi có ánh sáng.
Câu 3: Hỗn hợp A gồm CH4, C2H2 và một hiđrocacbon X có công thức CnH2n+2 .Cho 0,896 lít hỗn hợp A đi qua dung dịch brom dư để phản ứng xảy ra hoàn toàn, thấy thoát ra 0,448 lít hỗn hợp hai khí.
Biết rằng tỉ lệ số mol của CH4 và CnH2n+2 trong hỗn hợp là 1 : 1, khi đốt cháy 0,896 lít A thu được 3,08 gam khí CO2 (thể tích khí đo ở đktc).
a) Xác định công thức phân tử của hiđrocacbon X.
b) Tính thành phần phần trăm theo thể tích mỗi khí trong hỗn hợp A.
3.2. Bài tập trắc nghiệm
Câu 1: Hidrocacbon nào sau đây trong phân tử chỉ có liên kết đơn:
A. Etilen
B. Metan
C. Benzen
D. Axetilen
Câu 2: Chất nào sau đây khi tham gia phản ứng vừa có phản ứng cộng, vừa có phản ứng thế:
A. Metan
B. Benzen
C. Etilen
D. Axetilen
Câu 3: Câu nào sau đây đúng khi nói về dầu mỏ:
A. Dầu mỏ nặng hơn nước nên chìm dưới nước.
B. Dầu mỏ không tan trong nước.
C. Dầu mỏ tan nhiều trong nước.
D. Nhiệt độ sôi của dầu mỏ là 1000C
4. Kết luận
Sau bài học cần nắm:
- Các kiến thức đã học về hiđrocacbon.
- Hệ thống mối quan hệ giữa cấu tạo và tính chất của các hiđrocacbon.
Tham khảo thêm
- doc Hoá học 9 Bài 34: Khái niệm về hợp chất hữu cơ và hóa học hữu cơ
- doc Hoá học 9 Bài 35: Cấu tạo phân tử hợp chất hữu cơ
- doc Hoá học 9 Bài 36: Metan
- doc Hoá học 9 Bài 37: Etilen
- doc Hoá học 9 Bài 38: Axetilen
- doc Hoá học 9 Bài 39: Benzen
- doc Hoá học 9 Bài 40: Dầu mỏ và khí thiên nhiên
- doc Hoá học 9 Bài 41: Nhiên liệu
- doc Hoá học 9 Bài 43: Thực hành: Tính chất của Hiđrocacbon



