Hóa học 9 Bài 2: Một số oxit quan trọng
Nội dung bài học giúp học sinh tìm hiểu tính chất vật lý và hóa học của một số oxit quan trọng như canxi oxit, lưu huỳnh đi oxit. Đồng thời, biết các ứng dụng và cách điều chế các oxit đó.
Mục lục nội dung

1. Tóm tắt lý thuyết
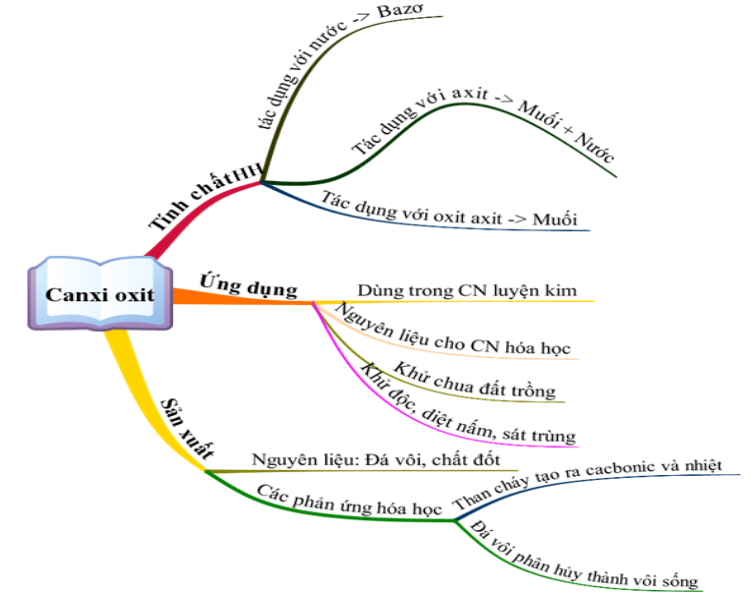
1.1. Canxi oxit (CaO)
a. Tính chất vật lý
Là chất rắn màu trắng, nóng chảy ở nhiệt độ rất cao (25850C).
b. Tính chất hóa học
Canxi oxit có đầy đủ tính chất của một oxit bazơ
- Tác dụng với nước:
Ca(OH)2 tan ít trong nước, phần tan tạo thành dung dịch bazơ.
CaO + H2O → Ca(OH)2
CaO có tính hút ẩm nên dùng để làm khô nhiều chất.
- Tác dụng với axit:
CaO + H2SO4 → CaSO4 + H2O (phản ứng tỏa nhiệt)
Nhờ tính chất này mà CaO được dùng để khử chua đất trồng trọt, xử lý nước thải của các nhà máy,...
- Tác dụng với oxit axit:
Vôi sống để lâu trong không khí không có lợi vì xảy ra phản ứng:
CaO + CO2 CaCO3
Để hạn chế phản ứng này người ta thường tôi vôi ngay sau khi nung.
c. Ứng dụng
Dùng trong công nghiệp luyện kim, nguyên liệu cho công nghiệp hóa học, khử chua đất trồng, xử lí nước thải, sát trùng,...
d. Sản xuất canxi oxit
- Nguyên liệu: đá vôi.
Chất đốt là than đá, củi, dầu, khí tự nhiên,...
- Các phản ứng hóa học xảy ra:
Than cháy tạo ra CO2, phản ứng tỏa nhiều nhiệt: C + O2 → CO2.
Nhiệt sinh ra phân hủy đá vôi thành vôi sống: CaCO3 CaO + CO2
1.2. Lưu huỳnh đioxit (SO2)
a. Tính chất vật lí
Lưu huỳnh đioxit là chất khí không màu, mùi hắc, độc, nặng hơn không khí.
b. Tính chất hóa học
SO2 mang đầy đủ tính chất của một oxit axit
- Tác dụng với nước:
Dẫn khí SO2 vào cốc đựng nước, sau đó thử dung dịch thu được bằng quỳ tím, thấy quỳ tím chuyển sang màu đỏ
Phương trình hóa học: SO2 + H2O → H2SO3
SO2 là chất gây ô nhiễm không khí, là một trong các nguyên nhân gây ra mưa axit.
- Tác dụng với bazơ:
Dẫn khí SO2 vào cốc đựng dung dịch Ca(OH)2 thấy xuất hiện kết tủa trắng (CaSO3)
Phương trình hóa học: SO2+ Ca(OH)2 → CaSO3 + H2O
- Tác dụng với oxit bazơ:
SO2 tác dụng với oxit bazơ (CaO, Na2O,...) tạo muối sunfit.
Phương trình hóa học: SO2 + Na2O → Na2SO3
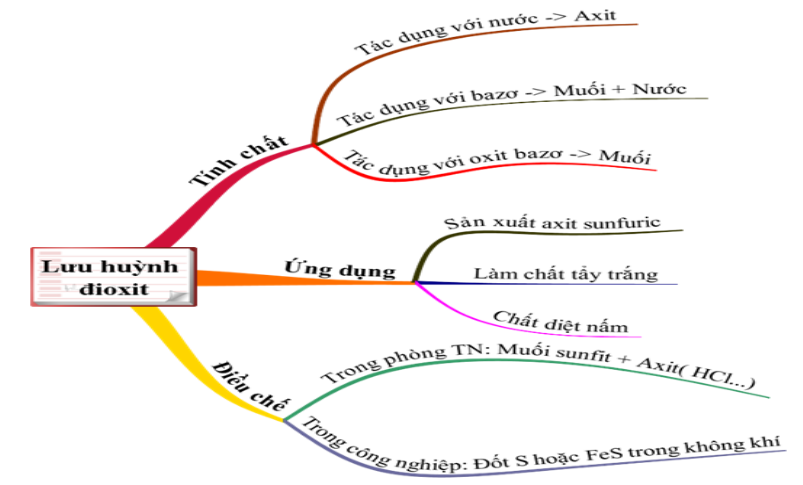
c. Ứng dụng
Phần lớn SO2 dùng để sản xuất H2SO4, dùng làm chất tẩy trắng bột gỗ, diệt nấm mốc,...
d. Điều chế lưu huỳnh đioxit
- Điều chế trong phòng thí nghiệm:
Cho muối sunfit tác dụng với dung dịch axit (HCl, H2SO4)
Phương trình hóa học: Na2SO3+H2SO4 → Na2SO4 + H2O + SO2
- Điều chế trong công nghiệp:
Đốt S trong không khí: S + O2 \(\xrightarrow{{{t^o}}}\) SO2
Đốt quặng pirit sắt (FeS2) thu được SO2 : 4FeS2 + 11O2 \(\xrightarrow{{{t^o}}}\) 2Fe2O3 + 8SO2
2. Bài tập minh họa
2.1. Dạng 1: Nhận biết chất rắn và chất khí
Nêu phương pháp hóa học nhận biết từng nhóm chất sau:
a) Hai chất rắn màu trắng là: CaO và P2O5
b) Hai chất khí không màu là SO2 và O2
Hướng dẫn giải
a) Cho mỗi chất tác dụng với nước, sau đó thử dung dịch thu được bằng quỳ tím, dung dịch nào làm quỳ chuyển sang màu xanh là dung dịch Ca(OH)2
⇒ Chất rắn là CaO, dung dịch làm quỳ chuyên sang màu đỏ là dung dịch H3PO4 ⇒ chất rắn là P2O5.
Phương trình hóa học:
CaO + H2O → Ca(OH)2
P2O5 + H2O → H3PO4
b) Dẫn lần lượt hai khí qua dung dịch nước vôi trong, khí nào làm đục nước vôi trong
⇒ khí đó là SO2, khí O2 không làm đục nước vôi trong.
Phương trình hóa học:
SO2 + Ca(OH)2 → CaSO4 + H2O
2.2. Dạng 2: Xác định khối lượng kết tủa trong phản ứng hóa học
Câu 1: Cho 5,6g CaO vào nước tạo thành dung dịch A. Tính số gam kết tủa tạo thành khi đem dung dịch A hấp thụ hoàn toàn 2,8 lít khí cacbonic.
Hướng dẫn giải
Số mol của CaO và CO2 bằng:
\(\begin{array}{*{20}{l}} {{n_{CaO}} = \frac{{\;5,6}}{{56}} = 0,1mol} \\ {{n_{CO2}} = \;\frac{{2,8}}{{22,4}}\; = 0,125mol} \end{array}\)
Ta có phương trình phản ứng:
CaO + H2O → Ca(OH)2
0,1mol 0,1mol
Ca(OH)2 + CO2 → CaCO3 + H2O
0,1mol 0,1mol 0,1mol
Số mol CO2 dư: 0,125 – 0,1 = 0,025 mol, sẽ tiếp tục phản ứng như sau:
CaCO3 + H2O + CO2 → Ca(HCO3)2
0,025mol 0,025mol 0,025mol
Khối lượng CaCO3 kết tủa là: (0,1 – 0,025).100 = 7,5 g.
Câu 2: Biết 2,24 lít khí CO2 (đktc) tác dụng vừa hết với 200 ml dung dịch Ba(OH)2 sản phẩm là BaCO3 và H2O:
a) Viết phương trình hóa học.
b) Tính nồng độ mol của dung dịch Ba(OH)2 đã dùng.
c) Tính khối lượng chất kết tủa thu được.
Hướng dẫn giải
a) Phương trình hóa học
CO2 + Ba(OH)2 → BaCO3↓ + H2O
b) nCO2= 2,24 / 22,4 = 0,1 mol
Dựa vào phương trình trên ta thấy:
nBa(OH)2 = nCO2 = 0,1 mol
⇒ CM Ba(OH)2 = 0,1 / 0,2 = 0,5 mol/l
c) Dựa vào phương trình, ta có:
nBaCO3 = nCO2 = 0,1 mol
⇒ mBaCO3 = 0,1 . 197 = 19,7 gam.
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: CaO là oxit bazơ, P2O5 là oxit axit. Chúng đều là những chất rắn, màu trắng. Bằng những phương pháp hoá học nào có thể giúp ta nhận biết được mỗi chất trên?
Câu 2: Cho 8 gam lưu huỳnh trioxit (SO3) tác dụng với H2O, thu được 250 ml dung dịch axit sunfuric (H2SO4)
a) Viết phương trình hoá học.
b) Xác định nồng độ mol của dung dịch axit thu được.
3.2. Bài tập trắc nghiệm
Câu 1: CaO để lâu trong không khí bị giảm chất lượng là vì:
A. CaO tác dụng với O2
B. CaO tác dụng với CO2
C. CaO dụng với nước
D. Cả B và C
Câu 2: CaO dùng làm chất khử chua đất trồng là ứng dụng tính chất hóa học gì của CaO?
A. Tác dụng với axit
B. Tác dụng với bazơ
C. Tác dụng với oxit axit
D. Tác dụng với muối
Câu 3: Sử dụng chất thử nào để phân biệt hai chất rắn màu trắng: CaO và P2O5
A. Dung dịch phenolphtalein
B. Giấy quỳ ẩm
C. Dung dịch axit clohiđric
D. A , B và C đều đúng
Câu 4: Oxit được dùng làm chất hút ẩm (chất làm khô) trong phòng thí nghiệm là:
A. CuO
B. ZnO
C. PbO
D. CaO
Câu 5: Dẫn hỗn hợp khí gồm CO2 , CO , SO2 lội qua dung dịch nước vôi trong (dư), khí thoát ra là :
A. CO
B. CO2
C. SO2
D. CO2 và SO2
4. Kết luận
Sau bài học cần nắm:
- Tính chất vật lý và hóa học của canxi oxit.
- Các ứng dụng và cách điều chế canxi oxit - lưu huỳnh đioxit.
- Khái quát về sự phân loại oxit đi sâu tìm hiểu tính chất hóa học và giúp học sinh nắm bắt được cơ sở phân loại oxit.
Tham khảo thêm
- docx Hoá học 9 Bài 1: Tính chất hóa học của oxit và Khái quát về sự phân loại oxit
- docx Hóa học 9 Bài 3: Tính chất hóa học của axit
- docx Hóa học 9 Bài 4: Một số axit quan trọng
- docx Hóa học 9 Bài 5: Luyện tập tính chất hóa học của oxit và axit
- docx Hóa học 9 Bài 6: Thực hành: Tính chất hóa học của oxit và axit
- docx Hóa học 9 Bài 7: Tính chất hóa học của bazơ
- docx Hóa học 9 Bài 8: Một số bazơ quan trọng
- docx Hóa học 9 Bài 9: Tính chất hóa học của muối
- doc Hóa học 9 Bài 10: Một số muối quan trọng
- docx Hóa học 9 Bài 11: Phân bón hóa học
- docx Hóa học 9 Bài 12: Mối quan hẹ giữa các loại hợp chất vô cơ
- docx Hóa học 9 Bài 13: Luyện tập chương 1 Các loại hợp chất vô cơ
- docx Hóa học 9 Bài 14: Thực hành: Tính chất hóa học của bazơ và muối



