Giải bài tập SGK Hóa 11 Nâng cao Bài 40: Anken - Tính chất, điều chế và ứng dụng
Dưới đây là Hướng dẫn giải Hóa 11 SGK nâng cao Chương 6 Bài 40 Anken - Tính chất, điều chế và ứng dụng được eLib biên soạn và tổng hợp, nội dung bám sát theo chương trình SGK Hóa học 11 nâng cao giúp các em học sinh nắm vững phương pháp giải bài tập và ôn tập kiến thức hiệu quả hơn.
Mục lục nội dung
1. Giải bài 1 trang 164 SGK Hóa học 11 nâng cao
2. Giải bài 2 trang 164 SGK Hóa học 11 nâng cao
3. Giải bài 3 trang 164 SGK Hóa học 11 nâng cao
4. Giải bài 4 trang 164 SGK Hóa học 11 nâng cao
5. Giải bài 5 trang 164 SGK Hóa học 11 nâng cao
6. Giải bài 6 trang 164 SGK Hóa học 11 nâng cao
7. Giải bài 7 trang 165 SGK Hóa học 11 nâng cao
8. Giải bài 8 trang 165 SGK Hóa học 11 nâng cao

1. Giải bài 1 trang 164 SGK Hóa 11 nâng cao
Hãy điền chữ Đ (đúng) hoặc chữ S (sai) vào dấu [...] ở mỗi câu sau:
a) Anken là chất kị nước. [...].
b) Anken là chất ưa dầu mỡ. [...].
c) Liên kết đôi kém bền hơn liên kết đơn. [...].
d) Liên kết π kém bền hơn liên kết σ. [...].
Phương pháp giải
Để giải bài tập này cần nắm vững đặc điểm, tính chất của anken
Hướng dẫn giải
a) Đúng
b) Đúng
c) Sai
d) Đúng
2. Giải bài 2 trang 164 SGK Hóa 11 nâng cao
Vì sao anken hoạt động hóa học hơn hẳn ankan? Hãy viết phương trình hóa học của propen dưới tác dụng của các tác nhân và điều kiện phản ứng sau:
a) Br2 trong CCl4
b) HI
c) H2SO4 98%
d)H2O/H+,to
e) KMnO4/H2O
g) Áp suất và nhiệt độ cao.
Phương pháp giải
- Trong phân tử có 1 liên kết đôi: gồm 1 liên kết σ và 1 liên kết π. Nguyên tử cacbon ở liên kết đôi tham gia 3 liên kết σ nhờ obitan lai hóa sp2, còn liên kết π nhờ obitan p không lai hóa.
- Do có liên kết pi nên khoảng cách giữa hai nguyên tử C=C ngắn lại và nguyên tử cacbon này không thể quay quanh liên kết đôi vì khi quay như vậy liên kết π bị phá vỡ.
Hướng dẫn giải
Anken hoạt động hóa học hơn hẳn ankan vì trong phân tử anken có chứa liên kết π kém bền nên có khả năng phản ứng dễ dàng.
CH3-CH=CH2 + Br2 → CH3-CH(Br)-CH2Br
CH3-CH=CH2 + HI → CH3-CH(I)-CH3
CH3-CH=CH2 + HI → CH3-CH2-CH2I
CH3-CH=CH2 + H2SO4 → CH3-CH(OSO3H)-CH3
CH3-CH=CH2 + H2SO4 → CH3-CH2-CH2OSO3H
CH3-CH=CH2 + H2O → CH3-CH(OH)-CH3
CH3-CH=CH2 + H2O → CH3-CH2-CH2OH
CH3-CH=CH2 + 2KMnO4 + 4H2O → CH3-CH(OH)-CH2OH
3. Giải bài 3 trang 164 SGK Hóa 11 nâng cao
a) Phản ứng trùng hợp là gì? Hệ số trùng hợp là gì? Cho ví dụ.
b) Viết sơ đồ phản ứng trùng hợp isobutilen và chỉ rõ monomer, mắt xích của polime và tính khối lượng mol phân tử trung bình của poliisobutilen nếu hệ số trùng hợp trung bình của nó là 15000.
Phương pháp giải
- Trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ (monome) giống nhau hay tương tự nhau thành phân tử lớn (polime).
- Hệ số trùng hợp là số mắt xích monomer hợp thành phân tử polime.
Hướng dẫn giải
Câu a:
- Trùng hợp là quá trình kết hợp liên tiếp nhiều phân tử nhỏ (monome) giống nhau hay tương tự nhau thành phân tử lớn (polime).
- Hệ số trùng hợp là số mắt xích monomer hợp thành phân tử polime. Polime là một hỗn hợp các phân tử với hệ số polime hóa không hoàn toàn như nhau. Vì vậy người ta chỉ khối lượng phân tử trung bình của polime và dùng hệ số polime hóa trung bình.
Ví dụ:
Monomer: CH2=C(CH3 )2
Mắt xích: -CH2-C(CH3 )2-
M = 15000.56 = 840000 đvC.
4. Giải bài 4 trang 164 SGK Hóa 11 nâng cao
Hidro hóa hoàn toàn một mẫu olefin thì hết 448ml H2 và thu được một ankan phân nhanh. Cũng lượng olefin đó khi tác dụng với brom thì tạo thành 4,32 gam dẫn xuất đibrom. Biết rằng hiệu suất của các phản ứng đạt 100% và thể tích khí đo ở đktc. Hãy xác định công thức cấu tạo, gọi tên olefin đã cho.
Phương pháp giải
Đặt công thức tổng quát của olefim là CnH2n
CnH2n + H2 → CnH2n+2 (1)
CnH2n + Br2 → CnH2nBr2 (2)
Từ (1) và (2) ⇒ số mol của dẫn xuất ⇒ n
Hướng dẫn giải
Đặt công thức tổng quát của olefim là CnH2n, số mol H2: 0,448/22,4 = 0,02 (mol)
CnH2n + H2 → CnH2n+2 (1)
0,02 0,02
CnH2n + Br2 → CnH2nBr2 (2)
0,02 0,02
Từ (1) và (2) ⇒ số mol của dẫn xuất là 0,02 mol
0,02.(14n + 160) = 4,32 ⇒ n = 4
Công thức cấu tạo của olefin :
CH2=C(CH3 )-CH3 (2-metyl propen)
5. Giải bài 5 trang 164 SGK Hóa 11 nâng cao
Có 3 anken A1, A2, A3 khi cho tác dụng với H2 có xúc tác Ni ở 50oC đều tạo thành 2-metylbutan. Hãy xác định công thức cấu tạo, gọi tên 3 anken đó và cho biết quan hệ đồng phân giữa chúng.
Phương pháp giải
A1, A2, A3 có cùng mạch C, chỉ khác vị trí nhóm chức C=C ⇒ đồng phân vị trí nhóm chức.
Hướng dẫn giải
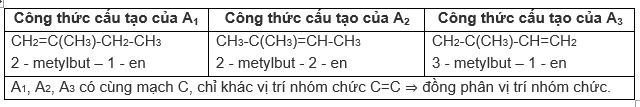
6. Giải bài 6 trang 164 SGK Hóa 11 nâng cao
Một hỗn hợp khí gồm 1 anken và 1 ankan có cùng số nguyên tử C trong phân tử và có cùng số mol. Hỗn hợp này vừa đủ làm mất màu 80 gam dung dịch 20% brom trong CCl4. Khi đốt cháy hoàn toàn hỗn hợp đó thì tạo thành 13,44 lít CO2 (đktc).
a) Xác định công thức cấu tạo của ankan và anken đã cho.
b) Xác định tỉ khối của hỗn hợp đó so với không khí.
Phương pháp giải
Đặt công thức tổng quát của ankan CnH2n+2; anken là CnH2n.
nBr2 = ?; nCO2 = ?
CnH2n + Br2 → CnH2nBr2 (1)
Theo pt: nCnH2n = nBr2 = ?
Theo bài ra ankan và anken có cùng số mol nên: nCnH2n = nCnH2n+2 = ?
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_n}{H_{2n}} + \frac{{3n}}{2}{O_2} \to nC{O_2} + n{H_2}O\)
Từ pt (2) và (3) ⇒ nCO2 = ?
⇒ Công thức cấu tạo của ankan, anken
⇒ Tỉ khối
Hướng dẫn giải
Đặt công thức tổng quát của ankan CnH2n+2; anken là CnH2n.
CnH2n + Br2 → CnH2nBr2 (1)
Theo pt: nCnH2n = nBr2 = 0,1 mol
Theo bài ra ankan và anken có cùng số mol nên: nCnH2n = nCnH2n+2 = 0,1 mol
\({C_n}{H_{2n + 2}} + \frac{{3n + 1}}{2}{O_2} \to nC{O_2} + (n + 1){H_2}O\)
\({C_n}{H_{2n}} + \frac{{3n}}{2}{O_2} \to nC{O_2} + n{H_2}O\)
Từ pt (2) và (3) ⇒ nCO2 = 0,1n + 0,1n = 0,6 ⇒ n = 3.
Công thức cấu tạo của ankan: CH3CH2CH3 propan
Công thức cấu tạo của anken: CH2=CHCH3 propen
Ta có:
\(\begin{array}{l}
\overline {{M_{hh}}} = \frac{{44.0,1 + 42.0,1}}{{0,2}} = 43g/mol\\
\to {d_{\frac{{hh}}{{kk}}}} = \frac{{\overline M }}{{29}} = \frac{{43}}{{29}} = 1,48
\end{array}\)
7. Giải bài 7 trang 165 SGK Hóa 11 nâng cao
2,8 gam anken A vừa đủ làm mất màu dung dịch chứa 8 gam Br2,
a) Viết phương trình hóa học (dùng công thức chung của anken CnH2n) và tính khối lượng mol phân tử của A.
b) Biết rằng hidrat hóa Anken A thì thu được chỉ một ancol duy nhất. hãy cho biết A có thể có cấu trúc như thế nào?
Phương pháp giải
CnH2n + Br2 → CnH2nBr2
nCnH2n = nBr2 = ? → MA
Ta có: MA = 14n → n = ?
→ Công thức phân tử của A
Hướng dẫn giải
Câu a: Đặt công thức tổng quát của anken A là CnH2n (n ≥ 2).
nBr2 = 0,05 mol
CnH2n + Br2 → CnH2nBr2
nCnH2n = nBr2 = 0,05 mol
Khối lượng mol phân tử của A:
MA = 2,8 : 0,05 = 56 g/mol
Câu b: Ta có MA = 56 ⇒ 14n = 56 ⇒ n = 4.
Công thức phân tử của A là C4H8
Khi hidrat hóa anken C4H8 chỉ thu được 1 ancol duy nhất suy ra anken có cấu tạo đối xứng ⇒ CTCT anken là CH3-CH=CH-CH3 (but-2-en)
Cấu trúc của A: cis-but-2-en và trans-but-2-en
8. Giải bài 8 trang 165 SGK Hóa 11 nâng cao
Có 3 ống nghiệm đều chứa dung dịch KMnO4 loãng. Cho vài giọt hexan vào ống nghiệm thứ nhất, vài giọt hex-1-en vào ống nghiệm thứ hai. Lắc đều cả 3 ống nghiệm, để yên thì thu được kết quả như ở hình 6.5.(SGK)
a) Ống nghiệm thứ nhất và thứ hai đã chuyển thành ống nghiệm nào ở hình 6.5?
b) Giải thích kết quả thí nghiệm và viết phương trình hóa học của phản ứng.

Phương pháp giải
Dựa vào khả năng phản ứng của một số hexan và hex-1-en để giải bài toán
Hướng dẫn giải
Câu a: Ống nghiệm thứ nhất chuyển thành ống nghiệm b vì hexan không tác dụng với KMnO4, không tan trong KMnO4 nên chúng tách thành hai lớp. Ống nghiệm thứ hai chuyển thành ống nghiệm c vì hex-1-en tác dụng với KMnO4, làm mất màu dung dịch KMnO4, tạo ra sản phẩm không tan, tách thành hai lớp.
Câu b: 3CH3-(CH2)3-CH=CH2 + 2KMnO4 + 4H2O→3CH3-(CH2)3-CHOH-CH2(OH) + 2KOH + 2MnO2.
9. Giải bài 9 trang 165 SGK Hóa 11 nâng cao
a) Viết công thức cấu trúc các hidrocacbon sinh ra khi đề hidro hóa butan với xúc tác ở nhiệt độ 500oC.
b) Nêu ý nghĩa của phản ứng trên.
Phương pháp giải
Hidrocacbon sinh ra là CH3-CH2-CH=CH2
Hướng dẫn giải
Câu a: CH3-CH2-CH2-CH3 → CH3-CH2-CH=CH2 + H2
Câu b: Ý nghĩa: phản ứng trên dùng để điều chế anken.
10. Giải bài 10 trang 165 SGK Hóa 11 nâng cao
Trong số 20 hóa chất được sản xuất nhiểu nhất H2SO4 đứng đầu, etilen chiến vị trí thứ tư, propilen đứng thứ 9, clo xếp thứ 10,… Hãy nêu lí do làm cho etilen và propilen chiếm được thứ bậc cao như vậy, dùng những phản ứng hóa học đề minh họa cho ý kiến của mình.
Phương pháp giải
Etilen và propilen chiếm được thứ bậc cao vì etilen, propilen là nguyên liệu quan trọng tổng hợp ra polime và các chất hữu cơ khác.
Hướng dẫn giải
Vì etilen , propilen là nguyên liệu quan trọng tổng hợp ra polime và các chất hữu cơ khác.
nCH2 = CH2 → (-CH2 - CH2-)n
nCH2 = CH - CH3 → (-CH2 - CH(CH3)-)n
CH2 = CH2 + HOH → CH3 - CH2 - OH
2CH2 = CH2 + O2 → CH2 - O- CH2
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 39: Anken - Danh pháp, cấu trúc và đồng phân
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 41: Ankađien
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 42: Khái niệm về tecpen
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 43: Ankin
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 44: Luyện tập hiđrocacbon không no



