Giải bài tập SGK Hóa 11 Nâng cao Bài 11: Amoniac và muối amoni
Dưới đây là Hướng dẫn giải Chương 2 Bài 11 Amoniac và muối amoni được eLib biên soạn và tổng hợp, nội dung bám sát theo chương trình SGK Hóa học 11 nâng cao giúp các em học sinh nắm vững phương pháp giải bài tập và ôn tập kiến thức hiệu quả hơn.
Mục lục nội dung
1. Giải bài 1 trang 47 SGK Hóa học 11 nâng cao
2. Giải bài 2 trang 47 SGK Hóa học 11 nâng cao
3. Giải bài 3 trang 47 SGK Hóa học 11 nâng cao
4. Giải bài 4 trang 47 SGK Hóa học 11 nâng cao
5. Giải bài 5 trang 47 SGK Hóa học 11 nâng cao
6. Giải bài 6 trang 47 SGK Hóa học 11 nâng cao

1. Giải bài 1 trang 47 SGK Hóa 11 nâng cao
Mô tả và giải thích hiện tượng xảy ra trong thí nghiệm chứng minh ammoniac tan nhiều trong nước.
Phương pháp giải
+ Amoniac tan nhiều trong nước tạo thành dung dịch amoniac có tính bazo → làm phenolphtalein chuyển sang màu hồng.
Hướng dẫn giải
- Mô tả thí nghiệm: Lắp thí nghiệm như hình vẽ
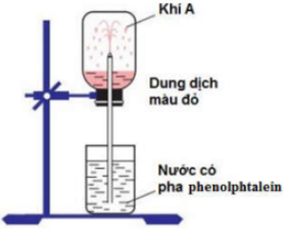
- Giải thích hiện tượng:
+ Amoniac tan nhiều trong nước tạo thành dd amoniac có tính bazo.
+ Do tan nhiều trong nước, áp suất của khí NH3 trong bình giảm đột ngột, nước trong cốc (có pha phenolphtalein) bị hút vào bình qua ống thủy tinh vuốt nhọn phun thành các tia màu hồng.
2. Giải bài 2 trang 47 SGK Hóa 11 nâng cao
Có 5 bình đựng riêng biệt 5 chất khi: N2,O2, NH3, Cl2 và CO2. Hãy đưa ra một thí nghiệm đơn giản để nhận ra bình đựng khi NH3.
Phương pháp giải
Có thể dùng 2 cách
+ Cách 1: Dùng dung dịch HCl
+ Cách 2: Dùng quỳ tím
Hướng dẫn giải
Cách 1: Dùng đũa thủy tinh nhúng vào lọ đựng dung dịch HCl và đưa vào lần lượt các bình mất nhãn trên nếu có khói trắng xuất hiện là bính đứng khi NH3:
NH3 + HCl → NH4Cl (rắn) khói trắng.
Cách 2: Dùng giấy quỳ tím tẩm nước tiếp xúc với miệng các bình khí. ở bình nào quỳ tím hóa xanh là NH3.
3. Giải bài 3 trang 47 SGK Hóa 11 nâng cao
Nêu tính chất hóa học đặc trưng và những ứng dụng của amoniac. Tại sao người ta nói amoniac là một bazơ yếu?
Phương pháp giải
Xem lại tính chất và ứng dụng của amoniac
+ Tính bazo yếu
+ Khả năng tạo phức
+ Tính khử
Hướng dẫn giải
- Tính chất hóa học của NH3
+ Tính bazơ yếu:
NH3 + H2O ⇔ NH4+ + OH-
NH3 + HCl → NH4Cl (bốc khói trắng)
AlCl3 + 3NH3 + H2O → Al(OH)3↓ + 3NH4Cl
Cu(NO3)2 + 2NH3 + H2O → Cu(OH)2↓ + 2NH4Cl
+ Khả năng tạo phức:
Cu(OH)2 + 4NH3 → [Cu(NH3 )4](OH)2
dung dịch xanh thẫm
+ Tính khử:
2NH3 + 3CuO → (to) 3Cu + N2 + 3H2O (2N3--6e → N2)
2NH3 + 3Cl2 → N2 + 6HCl (2N3--6e → N2 )
- Ứng dụng
+ NH3 được sử dụng để làm sản xuất HNO3 phân bón, điều chế N2H4 làm nhiên liệu cho tên lửa.
+ NH3 lỏng được dùng làm chất gây lạnh trong máy lạnh.
- NH3 là một bazơ yếu:
Với cùng nồng độ thì nồng độ OH- do NH3 tạo thành nhỏ hơn nhiều so với NaOH. NH3 bị bazơ đẩy ra khỏi dung dịch muối → NH3 là một bazơ yếu.
NH4NO3 + NaOH → NaNO3 + NH3 ↑ + H2O
4. Giải bài 4 trang 47 SGK Hóa 11 nâng cao
Dung dịch ammoniac có thể hòa tan được Zn(OH)2 là do
A. Zn(OH)2 là hiđroxit lưỡng tính.
B. Zn(OH)2 là một bazơ ít tan.
C. Zn(OH)2 có khả năng tạo thành phức chất tan tương tự như Cu(OH)2
D. NH3 là một hợp chất có cực là một bazơ yếu.
Phương pháp giải
+ Khả năng tạo phức:
Cu(OH)2 + 4NH3 → [Cu(NH3 )4](OH)2
dung dịch xanh thẫm
Hướng dẫn giải
Dung dịch amoniac có thể hòa tan được Zn(OH)2 là do Zn(OH)2 có khả năng tạo thành phức chất tan tương tự như Cu(OH)2
Zn(OH)2 + 4NH3 → [Zn(NH3)4](OH)2
Chọn C.
5. Giải bài 5 trang 47 SGK Hóa 11 nâng cao
Viết Phương trình hóa học của các phản ứng thực hiện sơ đồ chuyển hóa sau:
Khí A \(\xrightarrow{{{H_2}O}}\) dung dịch A \(\xrightarrow{{ + {\text{ }}HCl}}\) B \(\xrightarrow{{ + {\text{ }}NaOH}}\) khí A \(\xrightarrow{{ + HN{O_3}}}\) C \(\xrightarrow{{nung}}\) D + H2O
Phương pháp giải
Dựa vào tính chất hóa học và khả năng phản ứng của amoniac để hoàn thành sơ đồ phản ứng
NH3 \(\xrightarrow{{{H_2}O}}\) Dung dịch NH3\(\xrightarrow{{ + {\text{ }}HCl}}\) NH4Cl \(\xrightarrow{{ + {\text{ }}NaOH}}\) NH3 \(\xrightarrow{{ + HN{O_3}}}\) NH4NO3 \(\xrightarrow{{nung}}\)N2O + H2O
Hướng dẫn giải
Khí A là NH3
NH3 + H2O ⇔ NH4+ + OH-
khí A dung dịch A
NH3 + HCl → NH4Cl
(B)
NH4Cl + NaOH → NaCl + NH3 + H2O
(A)
NH3 + HNO3 → NH4NO3
(A) (C)
NH4NO3 → N2O + 2H2O
(C) (D)
6. Giải bài 6 trang 47 SGK Hóa 11 nâng cao
Cho cân bằng hóa học N2(k) + 3H2 (k) ⇔ 2NH3(k): ΔH = -92J
Cân bằng trên sẽ chuyển dịch theo chiều nào (có giải thích) khi:
a) Tăng nhiệt độ
b) Hóa lỏng ammoniac để tách ra khỏi hỗn hợp phản ứng.
c) Giảm thể tích của hệ Phương trình.
Phương pháp giải
Xem lại nguyên lí dịch chuyển cân bằng Lechateliter
Hướng dẫn giải
Theo nguyên lí dịch chuyển cân bằng Lechateliter:
- Khi tăng nhịêt độ cân bằng hóa học dịch chuyển theo chiều thu nhịêt. Tức chiều nghịch, chiều phân hủy NH3
- Khi hóa lỏng NH3 nồng độ NH3 giảm cân bằng hóa học sẽ dich chuyể theo chiều tăng làm nồng độ NH3 (chiều thuận) tạo thành NH3.
- Giảm thể tích của hỗn hợp phản ứng cân bằng hóa học dịch chuyển theo chiều giảm áp xuất (chiều thuận) tạo ra NH3.
7. Giải bài 7 trang 48 SGK Hóa 11 nâng cao
Có thể phân biệt muối ammoniac với các muối khác bằng cách cho nó tác dụng với dung dịch kiềm, vì khi đó:
A. Thoát ra một chất khi màu xanh lục nhạt.
B. Thoát ra một chất khí không màu, mùi khai, làm xanh quỳ tím ẩm.
C. Thoát ra một chất khí màu nâu đỏ, làm quỳ tím xanh ẩm.
D. Thoát ra chất khí không màu không mùi.
Hãy chọn đáp án đúng.
Phương pháp giải
Có thể phân biệt muối amoniac với các muối khác bằng cách cho nó tác dụng với dung dịch kiềm
Hướng dẫn giải
Có thể phân biệt muối amoniac với các muối khác bằng cách cho nó tác dụng với dung dịch kiềm, vì khi đó thoát ra một chất khí không màu, mùi khai, làm xanh quỳ tím ẩm.
NH4+ + OH- → NH3 + H2
→ Đáp án cần chọn là B.
8. Giải bài 8 trang 48 SGK Hóa 11 nâng cao
Người ta có ta có thể sản xuất amoniac để điều chế urê bằng cách chuyển hóa hữu cơ xúc tác một hỗn hợp gồm không khí, hơi nước và khí metan (thành phần chính của khí thiên nhiên).
Phản ứng điều chế H2 và CO2: CH4 + 2H2O → CO2 + 4H2 (1)
Phản ứng thu N2 (từ không khí) và CO2: CH4 + 2O3 → CO2 + 2H2O (2)
Phản ứng tổng hợp NH3: N2 + 3H2 ⇔ 2NH3 (3)
Để sản xuất khí aminiac, nếu lấy 841,7m3 không khí (chứa 21,03% O2, 78,02% N2, còn lại là khí hiếm), thì cần phải lấy bao nhiêu m3 khí metan và bao nhiêu m3 hơi nước để đủ năng lượng N2và H2 theo tỉ lệ 1: 3 về thể tích dùng cho phản ứng tổng hợp ammoniac. Giả thiết các phản ứng (1) và (2) đều xảy ra hoàn toàn và thể tích khí thu được đo ở điều kiện tiêu chuẩn
Phương pháp giải
- Bước 1: Tính thể tích khí O2 và N2 trong 841,7 m3 không khí
- Bước 2: Từ PTHH tính thể tích H2, CH4, H2O và thể tích H2O tạo thành
- Bước 3: Tính tổng thể tích CH4, H2O cần dùng
Hướng dẫn giải
Thể tích khí O2 và N2 trong 841,7 m3 không khí:
\(\begin{array}{l}
{V_{{O_2}}} = \frac{{841,7.21,03}}{{100}} = 177,01({m^3})\\
{V_{{H_2}}} = \frac{{841,7.78,02}}{{100}} = 656,69({m^3})
\end{array}\)
Từ pt (3) ta có: VH2 = 3.VN2 = 3.656,69 = 1970,08 m3
Từ pt (1) ta có: VCH4 = 1/4 . VH2 = 1979,08/4 = 492,52 m3
VH2O = 1/2 . VH2 = 1979,08/2 = 985,04 m3
Từ pt (2): VCH4 = 1/2 . VO2 = 177,01/2 = 88,5 m3
VH2O tạo thành = VO2 = 177,01 m3
⇒ Tổng VCH4 cần dùng là: 492,52 + 88,5 = 581,02 m3
⇒ Tổng VH2O cần dùng là: 985,04 – 177,01 = 808,039 m3
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 9: Khái quát về nhóm Nitơ
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 10: Nitơ
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 12: Axit nitric và muối nitrat
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 13: Luyện tập Tính chất của nitơ và hợp chất của nitơ
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 14: Photpho
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 15: Axit photphoric và muối photphat
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 16: Phân bón hóa học
- doc Giải bài tập SGK Hóa 11 Nâng cao Bài 17: Luyện tập Tính chất và các hợp chất của photpho



