Hoá học 11 Bài 40: Ancol
Nội dung bài giảng Ancol tìm hiểu về Định nghĩa, phân loại ancol; Công thức chung, đặc điểm cấu tạo phân tử, đồng phân, danh pháp (gốc - chức và thay thế). Tính chất vật lí : Nhiệt độ sôi, độ tan trong nước; Liên kết hiđro. Tính chất hoá học : Phản ứng của nhóm -OH (thế H, thế -OH), phản ứng tách nước tạo thành anken hoặc ete, phản ứng oxi hoá ancol bậc I, bậc II thành anđehit, xeton ; Phản ứng cháy. Phương pháp điều chế ancol từ anken, điều chế etanol từ tinh bột, điều chế glixerol. Ứng dụng của etanol. Công thức phân tử, cấu tạo, tính chất riêng của glixerol (phản ứng với Cu(OH)2).
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Định nghĩa, phân loại
a. Định nghĩa
Ancol là hợp chất hữu cơ mà trong phân tử có nhóm hiđroxyl (-OH) liên kết trực tiếp với nguyên tử cacbon no của gốc hiđrocacbon.
Ví dụ: CH3OH, C2H5OH, CH3CH2CH2OH, CH2=CHCH2OH, C6H5CH2OH ...
b. Phân loại
Phân loại Ancol
+ Theo gốc hidrocacbon
+ Theo số nhóm -OH
+ Theo bậc ancol
Một số loại ancol tiêu biểu
Ancol no mạch hở, đơn chức: có nhóm -OH liên kết trực tiếp với gốc ankyl
VD: CH3OH, C2H5OH,...,CnH2n - OH
Ancol không no, mạch hở, đơn chức: có nhóm -OH liên kết với nguyên tử cacbon của gốc hiđrocacbon không no
VD: CH2 = CH - CH2 - OH
Ancol thơm đơn chức: có nhóm -OH liên kết với nguyên tử cacbon no thuộc mạch nhánh của vòng Benzen
VD: C6H5 - CH2 - OH: ancolbenzylic
Ancol vòng no, đơn chức: có nhóm -OH liên kết với nguyên tử cacbon no thuộc hiđrocacbon vòng no
VD: 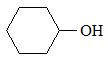 xiclohexanol
xiclohexanol
Ancol đa chức: phân tử có hai hay nhiều nhóm -OH
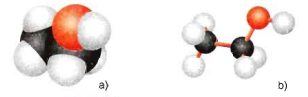
VD: CH2OH-CH2OH (Etilen glicol); CH2OH-CHOH-CH2OH (glixerol)
1.2. Đồng phân danh pháp
a. Đồng phân
- Có 2 loại:
+ Đồng phân về vị trí nhóm chức
+ Đồng phân về mạch cacbon
b. Danh pháp
Tên thông thường (gốc - chức)
Ví dụ:
CH3 - OH (Ancol metylic)
CH3 - CH2 - OH (ancol etilic)
CH3 - CH2 - CH2 - OH (ancol propylic)
Nguyên tắc: Ancol + tên gốc ankyl + ic
Tên thay thế
Ví dụ:
CH3-OH: metanol
CH3-CH2-OH: Etanol
CH3-CH2-CH2-CH2-OH: butan-1-ol
CH3-CH(CH3)-CH2-OH : 2-metylpropan-1-ol
Chú ý:
Mạch chính được quy định là mạch cacbon dài nhất chứa nhóm OH.
Số chỉ vị trí được bắt đầu từ phía gần nhóm -OH hơn.
Nguyên tắc: Tên hidrocacbon tương ứng mạch chính + số chỉ vị trí nhóm OH (nếu có) + "ol"
1.3. Tính chất vật lí
Ancol là chất lỏng hoặc rắn, tan được trong nước
Độ tan tỉ lệ nghịch với phân tử khối
Nhiệt độ sôi tỉ lệ thuận với phân tử khối.
Liên kết hiđro: Nguyên tử H mang một phần điện tích dương \({\delta ^ + }\) của nhóm -OH này khi ở gần nguyên tử O mang một phần điện tích \({\delta ^ - }\) của nhóm -OH kia thì tạo thành một liên kết yếu gọi là liên kết hiđro, biểu diễn bằng dấu...
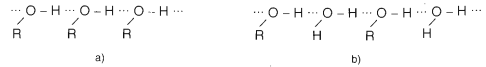
a) Giữa các phân tử ancol với nhau
b) Giữa các phân tử ancol với các phân tử nước
Ảnh hưởng của liên kết hiđro đến tính chất vật lí: liên kết hidro làm cho ancol có nhiệt độ sôi cao hơn, tan nhiều trong nước hơn.
1.4. Tính chất hóa học
Trong phân tử, liên kết C-OH đặc biệt liên kết O-H phân cực mạnh nên nhóm -OH, nhất là nguyên tử H dễ bị thay thế hoặc tách ra trong phản ứng hóa học.
a. Phản ứng thế H của nhóm -OH
Tính chất chung của ancol
Tác dụng với kim loại kiềm:
Phương trình tổng quát: R-OH+ Na(K)→R-ONa + 1/2H2
Video 1: Phản ứng của etanol với Natri
Natri phản ứng với etanol tạo khí hidro: 2C2H5-OH +2Na →2C2H5-ONa + H2
Đốt khí thoát ra ở đầu vuốt nhọn, hidro cháy với ngọn lửa xanh mờ:
2H2 + O2 → H2O
Tính chất đặc trưng của glixerol
Phản ứng này cần sử dụng Cu(OH)2 mới sinh, do đó khi cần tiến hành thí nghiệm người ta mới điều chế Cu(OH)2
Phương trình phản ứng:
CuSO4 + 2NaOH → Cu(OH)2 + Na2SO4
Hòa tan Cu(OH)2 tạo dd màu xanh lam.
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu +2H2O.
Đồng (II)glixerat
2.png)
Video 2: Glixerol tác dụng với Cu(OH)2
⇒ Phản ứng này được dùng để phân biệt ancol đơn chức với ancol đa chức có các nhóm -OH cạnh nhau trong phân tử.
b. Phản ứng thế nhóm -OH
Phản ứng với axit vô cơ
C2H5-OH + HBr → C2H5-Br + H2O
Phản ứng với ancol
C2H5-OH + H-OC2H5 → C2H5-O-C2H5 + H2O
đietyl ete (ete etylic)
c. Phản ứng tách nước
CH3-CH2-OH → CH2=CH2 + H2O
⇒ Tính chất này được ứng dụng để điều chế anken từ các ankanol
d. Phản ứng oxi hóa
Oxi hóa không hoàn toàn
Ancol bậc 1→ andehit (-CH→O)
VD: C2H5OH + CuO → CH3-CHO + H2O.
Ancol bậc 2: → xetôn (>C→O)
VD: CH3-CH(OH)-CH3 + CuO → CH3-CO-CH3 + H2O
Trong điều kiện như trên các ancol bậc 3 không bị oxi hóa.
Oxi hóa hoàn toàn
Cháy tỏa nhiều nhiệt
Phương trình tổng quát:
CnH2n+1-OH + 3n/2O2 → nCO2 + (n+1)H2O
1.5. Điều chế
a. Phương pháp tổng hợp
Etanol tổng hợp từ etylen: C2H4 + H2O → C2H5-OH
Tổng hợp ancol bằng cách thủy phân dẫn xuất halogen:
C2H5-Br + NaOH → C2H5-OH+ NaBr
Glixerol tổng hợp từ propilen
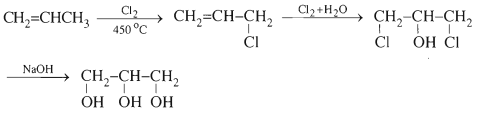
b. Phương pháp sinh hóa
(C6H10O5)n + nH2O → nC6H12O6
C6H12O6 → 2C2H5OH + 2CO2
1.6. Ứng dụng
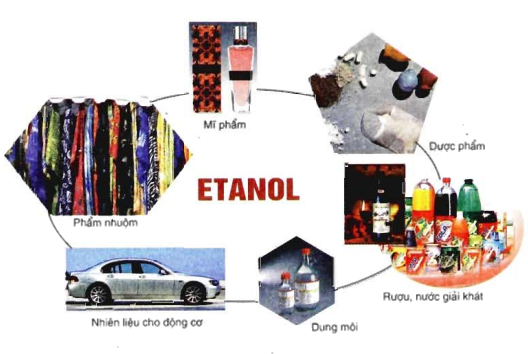
2. Bài tập minh họa
2.1. Dạng 1: Ancol tách nước
Bài 1: Đun 132,8 gam hỗn hợp 3 rượu no, đơn chức với H2SO4 đặc ở 140oC thu được hỗn hợp các ete có số mol bằng nhau và có khối lượng là 111,2 gam. Số mol của mỗi ete trong hỗn hợp là bao nhiêu ?
A. 0,1 mol.
B. 0,15 mol.
C. 0,4 mol.
D. 0,2 mol.
Hướng dẫn giải
Ta biết rằng cứ 3 loại rượu tách nước ở điều kiện H2SO4 đặc, 140oC thì tạo thành 6 loại ete và tách ra 6 phân tử H2O.
Theo ĐLBTKL ta có
mH2O = mrượu – mete = 132,8 – 111,2 = 21,6g
⇒ nH2O = 1,2 mol = nete
nmỗi ete = 1,2/6 = 0,2 mol ⇒ Đáp án D
Bài 2: Tách nước hỗn hợp gồm ancol etylic và ancol Y chỉ tạo ra 2 anken. Đốt cháy cùng số mol mỗi ancol thì lượng nước sinh ra từ ancol này bằng 5/3 lần lượng nước sinh ra từ ancol kia. Công thức cấu tạo của Y là:
A. CH3-CH2-CH2-OH.
B. CH3-CH(OH)-CH3.
C. CH3-CH2-CH2-CH2-OH.
D. CH3-CH2-CH(OH)-CH3.
Hướng dẫn giải
Gọi công thức ancol Y là: CnH2n+2O ( đáp án tất cả là ancol no đơn chức)
C2H6O → 3H2O
CnH2n+2O → (n+1)H2O
Ta có: (n+1)/3 = 5/3 ⇒ n = 4: C4H10O
Tách nước hỗn hợp gồm ancol etylic và ancol Y chỉ tạo ra 2 anken
⇒ Công thức cấu tạo của Y: CH3-CH2-CH2-CH2-OH
⇒ Đáp án C
2.2. Dạng 2: Ancol tác dụng với Na
Cho 13,8 gam ancol A tác dụng với Na dư giải phóng 5,04 lít H2 ở đktc, biết MA < 100. Vậy A có công thức cấu tạo thu gọn là :
A. CH3OH.
B. C2H5OH.
C. C3H6(OH)2.
D. C3H5(OH)3.
Hướng dẫn giải
Đặt công thức của ancol là R(OH)n.
Phương trình phản ứng :
2R(OH)n + 2Na → 2R(ONa)n + nH2 (1)
13,8/(R+17n) →
13,8/(R+17n). n/2 (mol)
Theo (1) và giả thiết ta có : nH2 = 13,8/(R+17n). n/2 = 0,225 mol
⇒ R = 41/3n ⇒ n = 3; R = 41
Vậy A có công thức cấu tạo thu gọn là C3H5(OH)3
⇒ Đáp án D
2.3. Dạng 3: Ancol bị oxi hóa không hoàn toàn
Bài 1: Oxi hóa 6 gam ancol đơn chức A bằng oxi không khí (có xúc tác và đun nóng) thu được 8,4 gam hỗn hợp anđehit, ancol dư và nước. Phần trăm A bị oxi hóa là :
A. 60%.
B. 75%.
C. 80%.
D. 53,33%.
Hướng dẫn giải
Đặt công thức của ancol là RCH2OH.
Số mol O2 đã tham gia phản ứng là : nO2 = (8,4-6)/32 = 0,075 mol
Phương trình phản ứng :
2RCH2OH + O2 → 2RCHO + 2H2O (1)
0,15 0,075 (mol)
Theo (1) ta thấy số mol RCH2OH đã phản ứng là 0,15 mol, theo giả thiết sau phản ứng ancol còn dư nên ta suy ra số mol ancol ban đầu phải lớn hơn 0,15 mol.
⇒ 6/MA > 0,15 ⇒ MA < 40 ⇒ R < 9
⇒R là H, ancol A là CH3OH.
H% = 0,15.32/6.100% = 80%
⇒ Đáp án C
Bài 2: Cho m gam một ancol (rượu) no, đơn chức X qua bình đựng CuO (dư), nung nóng. Sau khi phản ứng hoàn toàn, khối lượng chất rắn trong bình giảm 0,32 gam. Hỗn hợp hơi thu được có tỉ khối đối với hiđro là 15,5. Giá trị của m là?
Hướng dẫn giải
Đặt công thức phân tử của ancol no, đơn chức X là : CnH2n + 2O
Phương trình phản ứng :
CnH2n + 2O + CuO → CnH2nO + H2O + Cu (1)
x x → x → x → x (mol)
mc/r giảm = mCuO – mCu = 80x – 64x = 0,32 => x = 0,02
Hỗn hợp hơi gồm CnH2nO và H2O có M=15,5.2 = 31 và n = 0,02.2 = 0,04 mol.
Áp dụng định luật bảo toàn khối lượng ta có :
mancol = mhỗn hợp hơi + mCu – mCuO
mancol = 0,04.31 + 0,02,64 – 0,02.80 = 0,92 gam
2.4. Dạng 4: Đốt cháy ancol
Đốt cháy hoàn toàn 0,2 mol một ancol X no, mạch hở cần vừa đủ 17,92 lít khí O2 (ở đktc). Mặt khác, nếu cho 0,1 mol X tác dụng vừa đủ với m gam Cu(OH)2 thì tạo thành dung dịch có màu xanh lam. Giá trị của m và tên gọi của X tương ứng là :
A. 9,8 và propan-1,2-điol.
B. 4,9 và propan-1,2-điol.
C. 4,9 và propan-1,3-điol.
D. 4,9 và glixerol
Hướng dẫn giải
Đặt công thức phân tử của ancol no X là CnH2n + 2Ox (x n).
Phương trình phản ứng :
CnH2n+2Ox + (3n+1-x)/2O2 to→ nCO2 + (n+1)H2O (1)
0,2 → (3n+1-x)/2 .0,2 (mol)
⇒ (3n+1-x)/2 .0,2 = 0,8 mol ⇒ 3n – x = 7
⇒ x = 2; n = 3
Vậy công thức phân tử của ancol X là C3H8O2 hay C3H6(OH)2. Vì X tác dụng được với Cu(OH)2 tạo ra dung dịch màu xanh lam nên X phải có 2 nhóm OH liền kề nhau, ancol X có tên là propan-1,2-điol.
Phương trình phản ứng của propan-1,2-điol với Cu(OH)2 :
2C3H6(OH)2 + Cu(OH)2 → [C3H6(OH)O]2Cu + 2H2O (2)
0,1 0,05 (mol)
Theo (2) và giả thiết ta thấy khối lượng Cu(OH)2 phản ứng là :
mCu(OH)2 = 0,05.98 = 4,9g
⇒ Đáp án B.
2.5. Dạng 5: Ancol phản ứng với axit
Đun nóng ancol A với hỗn hợp NaBr và H2SO4 đặc thu được chất hữu cơ B, 12,3 gam hơi chất B chiếm một thể tích bằng thể tích của 2,8 gam N2 ở cùng nhiệt độ 560oC, áp suất 1 atm. Oxi hoá A bằng CuO nung nóng thu được hợp chất hữu cơ có khả năng làm mất màu dung dịch nước brom. CTCT của A là :
A. CH3OH.
B. C2H5OH.
C. CH3CHOHCH3.
D. CH3CH2CH2OH
Hướng dẫn giải
Phương trình phản ứng :
NaBr + H2SO4 → NaHSO4 + HBr (1)
ROH + HBr → RBr + H2O (2)
(A) (B)
Theo các phản ứng và giả thiết ta có :
nRBr = nN2 = 2,8/28 = 0,1 mol
=> MRBr = 12,3/0,1 = 123 gam/mol => R = 43
⇒ R là C3H7–
Vậy ancol A là C3H7OH. Vì oxi hóa A bằng CuO thu được hợp chất hữu cơ có khả năng làm mất màu nước Br2 nên công thức cấu tạo của A là CH3CH2CH2OH.
CH3CH2CH2OH + CuO → CH3CH2CHO (3)
CH3CH2CHO + Br2 + H2O → CH3CH2COOH + 2HBr (4)
⇒ Đáp án D
2.6. Dạng 6: Điều chế ancol etylic
Lên men m gam glucozơ với hiệu suất 90%, lượng khí CO2 sinh ra hấp thụ hết vào dung dịch nước vôi trong, thu được 10 gam kết tủa. Khối lượng dung dịch sau phản ứng giảm 3,4 gam so với khối lượng dung dịch nước vôi trong ban đầu. Giá trị của m là :
A. 20,0.
B. 30,0.
C. 13,5.
D. 15,0.
Hướng dẫn giải
Phương trình phản ứng :
C6H12O6 lên men rượu→ 2C2H5OH + 2CO2 (1)
CO2 + Ca(OH)2 → CaCO3 + H2O (2)
2CO2 + Ca(OH)2 → Ca(HCO3)2 (3)
mdung dịch giảm = mCaCO3 kết tủa – mCO2
⇒ mCO2 = mCaCO3 – mdung dịch giảm = 6,6g ⇒ nCO2 = 0,15 mol
Theo (1) ta có :
nC6H12O6 pư = 1/2 nCO2 = 0,075 mol
Vì hiệu suất phản ứng lên men là 90% nên lượng glucozơ cần cho phản ứng là :
nC6H12O6 pư = 0,075 : 90% = 1/12 mol ⇒ m = 1/12.180 = 15g
⇒ Đáp án D.
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Sản phẩm chính thu được khi tách nước từ 3-metylbutan-2-ol là gì, viết phương trình hóa học?
Câu 2: Hai ancol X, Y đều có CTPT C3H8O số anken thu được khi đun hỗn hợp X và Y với dung dịch H2SO4 đặc ở nhiệt độ cao là?
Câu 3: Đốt cháy hoàn toàn m gam hỗn hợp 3 ancol đơn chức, thuộc cùng dãy dồng đẳng thu được 3,808 lít khí CO2 (đktc) và 5,4 gam H2O. Giá trị của m là?
Câu 4: Từ 180 gam glucozo, bằng phương pháp lên men rượu, thu được a gam ancol etylic (hiệu suất 80%). Oxi hóa 0,1a gam ancol etylic bằng phương pháp lên men giấm, thu được hỗn hợp X. đẻ trung hòa hỗn hợp X cần 720 ml dung dịch NaOH 0,2M. Hiệu suất quá trình lên men giấm là?
Câu 5: Thực hiện phản ứng lên men m gam glucozơ thu được 750 ml rượu 10o. Biết khối lượng riêng của rượu là: 0,7907 g/ml và hiệu suất phản ứng lên men rượu là 60%. Giá trị m là?
3.2. Bài tập trắc nghiệm
Câu 1: Tên thay thế của C2H5OH là
A. ancol etylic
B. ancol metylic
C. etanol
D. metanol.
Câu 2: Cho các ancol sau: CH3OH, C2H5OH, HOCH2-CH2OH, HOCH2-CH2-CH2OH, CH3-CH(OH)-CH2OH. Số anncol cho ở trên phản ứng được với Cu(OH)2 ở nhiệt độ thường là
A. 2
B. 3
C. 4
D. 5
Câu 3: Oxi hóa ancol nào sau đây không tạo anđehit ?
A. CH3OH.
B. (CH3)2CHCH2OH.
C. C2H5CH2OH
D. CH3CH(OH)CH3.
Câu 4: Hiđrat hóa 2 anken chỉ tạo thành 2 ancol. Hai anken đó là
A. 2-metylpropen và but-I-en.
B. propen và but-2-en.
C. eten và but-2-en
D. eten và but-I-en.
Câu 5: Khi tách nước từ một chất X có công thức phân tử C4H10O tạo thành ba anken là đồng phân của nhau (tính cả đồng phân hình học). Công thức cấu tạo thu gọn của X là
A. (CH3)2COH).
B. CH3OCH2CH2CH3.
C. CH3CH(OH)CH2CH3.
D. CH3CH(CH3)CH2OH.
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Ancol Hóa học 11 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Sau bài học cần nắm:
- Đặc điểm cấu tạo của ancol
- Quan hệ giữa đặc điểm cấu tao với tính chất vật lí (nhiệt độ sôi, tính tan)
- Tính chất hoá học
- Phương pháp điều chế ancol
Tham khảo thêm
- doc Hoá học 11 Bài 39: Dẫn xuất halogen của hiđrocacbon
- doc Hoá học 11 Bài 41: Phenol
- doc Hoá học 11 Bài 42: Luyện tập Dẫn xuất halogen, ancol, phenol
- doc Hoá học 11 Bài 43: Bài thực hành 5 Tính chất của etanol, glixerol và phenol



