Hoá học 10 Bài 14: Tinh thể nguyên tử và tinh thể phân tử
Nội dung bài giảng Tinh thể nguyên tử và tinh thể phân tử tìm hiểu thế nào là tinh thể nguyên tử? Tinh thể phân tử? Tính chất chung của tinh thể nguyên tử, tinh thể phân tử.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Tinh thể nguyên tử
a. Tinh thể nguyên tử
- Than chì:
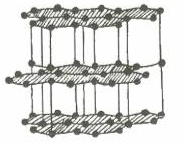
+ Tính chất vật lý: Tinh thể màu xám đen, dẫn điện dẫn nhiệt tốt. mềm
+ Cấu trúc: Cấu trúc lớp, các lớp liên kết nhau bằng tương tác yếu.
+ Ứng dụng: Làm điện cực, làm nồi để nấu chảy hợp kim chịu nhiệt, chế tạo chất bôi trơn, bút chì đen ...
- Kim cương:
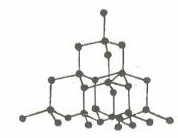
+ Tính chất vật lý: Tinh thể trong suốt, không màu, không dẫn điện, dẫn nhiệt kém, rất cứng, là chất cứng nhất trong tất cả các chất.
+ Cấu trúc: Tứ diện đều, liên kết cộng hóa trị bền
+ Ứng dụng: Làm đồ tráng sức, chế tạo mũi khoan,dao cắt thủy tinh, làm bột mài...
b. Tính chất chung của tinh thể nguyên tử
- Lực liên kết cộng hóa trị trong tinh thể nguyên tử rất lớn. Vì vậy, tinh thể bền vững, rất cứng, nhiệt độ nóng chảy và nhiệt độ sôi khá cao.
- Kim cương có độ cứng lớn nhất so với các tinh thể đã biết nên quy ước có độ cứng là 10 đơn vị. Đó là đơn vị để so sánh độ cứng của các chất.
1.2. Tinh thể phân tử
a. Tinh thể phân tử
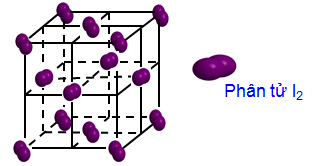
- Tại nút mạng tinh thể là các phân tử I2.
- Các phân tử I2 trong tinh thể hút nhau bằng lực tương tác yếu.
- Tinh thể iot (I2) là tinh thể phân tử, ở nhiệt độ thường iot ở thể rắn với cấu trúc tinh thể mạng lưới lập phương tâm diện: các phân tử iot ở 8 đỉnh và ở các tâm 6 mặt của hình lập phương.
b. Tính chất chung của tinh thể phân tử
- Trong tinh thể phân tử, các phân tử vẫn vốn tồn tại như những đơn vị độc lập và hút nhau bằng lực tương tác yếu giữa các phân tử. Vì vậy, tinh thể phân tử dễ nóng chảy, dễ bay hơi.
- Các tinh thể phân tử không phân cực dễ hòa tan trong các dung môi không phân cực như Benzen, toluen, cacbon tetraclorua...
2. Bài tập minh họa
So sánh tinh thể ion, tinh thể nguyên tử và tinh thể phân tử?
Hướng dẫn giải
- Ion:
+ Nút mạng: Các ion âm và ion dương
+ Lực liên kết: Lực hút tĩnh điện lớn
+ Tính chất chung: Bền vững; to nóng chảy , to sôi cao
- Nguyên tử:
+ Nút mạng: Nguyên tử
+ Lực liên kết: Lực liên kết cộng hoá trị lớn
+ Tính chất chung: Cứng, to nóng chảy , to sôi cao
- Phân tử:
+ Nút mạng: Phân tử
+ Lực liên kết: Lực tương tác yếu giữa các phân tử
+ Tính chất chung: Mềm, to nóng chảy, to sôi thấp
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Người ta có thể dùng dao để cắt kính, mũi khoan để khoan được các vật rất cứng là do đầu mũi dao và khoan có gắn?
Câu 2: Trong tinh thể kim cương, mỗi nguyên tử C liên kết với bao nhiêu nguyên tử cacbon lân cân gần nhất?
Câu 3: Cấu trúc của tinh thể phân tử nước đá thuộc loại cấu trúc nào?
Câu 4: Iot có thể chuyển thẳng từ thể rắn sang thể hơi gọi là hiện tượng?
Câu 5: Tại sao khi cho đá vào cốc nước ta thấy đá nổi lên?
3.2. Bài tập trắc nghiệm
Câu 1: Tinh thể nào sau đây là tinh thể nguyên tử
A. Iot
B. Băng phiến
C. Nước đá
D. Kim cương
Câu 2: Khẳng định nào sau đây là đúng:
A. Tinh thể nguyên tử là tinh thể tạo bởi các nguyên tử nằm ở các nút mạng, liên kết với nhau bằng liên kết cộng hóa trị
B. Tinh thể nguyên tử là tinh thể tạo bởi các nguyên tử nằm ở các nút mạng, liên kết với nhau bằng liên kết ion
C. Các tinh thể nguyên tử đều có độ cứng nhỏ, nhiệt độ sôi và nhiệt độ nóng chảy thấp
D. Liên kết trong tinh thể là liên kết kém bền
Câu 3: Khẳng định nào sau đây sai:
A. Lực tương tác giữa các phân tử trong tinh thể phân tử rất yếu
B. Cấu tạo tinh thể thường mềm
C. Tinh thể phân tử có nhiệt độ nóng chảy thấp, dễ bay hơi
D. Trong tinh thể phân tử, liên kết giữa các phân tử là liên kết cộng hóa trị
Câu 4: Đặc điểm nào sau đây là đặc điểm về cấu trúc và liên kết trong tinh thể iot:
A. Các nguyên tử I2 phân bố ở các đỉnh và tâm ở các mặt của hình lập phương
B. Các phân tử I2 phân bố ở các đỉnh và tâm ở các mặt của hình lập phương
C. Các phân tử I2 liên kết với nhau bằng liên kết cộng hóa trị
D. Các nguyên tử I2 liên kết với nhau bằng lực tương tác yếu giữa các nguyên tử
Câu 5: Trong các tinh thể sau tinh thể nào là tinh thể phân tử
A. Silic
B. Kim cương
C. Nước đá
D. Gemani
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Tinh thể nguyên tử và tinh thể phân tử Hóa học 10 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Sau bài học cần nắm:
- Tinh thể nguyên tử? Tinh thể phân tử?
- Tính chất chung của tinh thể nguyên tử, tinh thể phân tử.
Tham khảo thêm
- doc Hoá học 10 Bài 12: Liên kết ion - Tinh thể ion
- doc Hoá học 10 Bài 13: Liên kết cộng hóa trị
- doc Hoá học 10 Bài 15: Hóa trị và số oxi hóa
- doc Hoá học 10 Bài 16: Luyện tập Liên kết hóa học



