Hoá học 8 Bài 32: Phản ứng oxi hóa - khử
Qua bài học hiđro, các em đã hiểu tính chất của hiđro, ứng dụng của hiđro. Như vậy hiđro là chất đóng vai trò như thế nào trong phản ứng oxi hoá- khử? Để hiểu rõ hơn tiết học này các em sẽ tìm hiểu.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Sự khử và sự oxi hóa
a. Sự khử
- Sự khử là sự tách oxi ra khỏi hợp chất. (Chất khử là chất nhường electron, chất oxy hóa là chất nhận electron)
b. Sự oxi hóa
- Sự oxi hóa là sự tác dụng của oxi với một chất.
1.2. Chất khử và chất oxi hóa
- Chất khử là chất chiếm oxi của chất khác.
- Chất oxi hóa là chất nhường oxi cho chất khác.
1.3. Phản ứng oxi hóa - khử
- Phản ứng oxi hóa – khử là phản ứng hóa học xảy ra đồng thời sự oxi hóa và sự khử.
- Trong phương trình hóa học: CuO + H2 → Cu + H2O
- Có thể biểu diễn quá trình khử và oxi hóa của phản ứng CuO + H2 như sau:
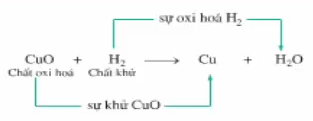
⇒ Sự khử và sự oxi hóa là 2 quá trình trái ngược nhau, nhưng xảy ra đồng thời trong 1 phương trình hóa học.
? Phản ứng sau có phải là phản ứng oxi hoá – khử không ? Vì sao ?
2H2 + O2 → 2H2O
Dựa vào dấu hiệu có sự nhường và chiếm oxi giữa các chất để phân biệt phản ứng oxi hóa với các loại phản ứng khác.
2. Bài tập minh họa
2.1. Dạng 1: Cách xác định loại phản ứng hóa học
Bài 1: Phản ứng nào sau đây là phản ứng oxi hóa – khử?
A. Fe2 O3 + 6HNO3 → 2Fe(NO3 ) 3 + 3H2 O
B. H2 SO4 + Na2 O → Na2 SO4 + 2H2 O
C. Fe2 O3 + 3CO → 2Fe + 3CO2
D. 2AgNO3 + BaCl2 → Ba(NO3 ) 2 + 2AgCl ↓
Hướng dẫn giải
Nhắc lại: Phản ứng oxi hóa khử là phản ứng có sự thay đổi số oxi hóa.
Xét sự thay đổi số oxi hóa của các chất trong các phản ứng trên ta thấy chỉ có đáp án C có sự thay đổi số oxi hóa Fe3+ xuống Fe0; C+2 lên C+4
⇒ Chọn C
Bài 2: Phản ứng nào sau đây vừa là phản ứng hóa hợp, vừa là phản ứng oxi hóa – khử?
A. CaO + H2 O → Ca(OH) 2
B. 2NO2 → N2 O4
C. 2NO2 + 4Zn → N2 + 4ZnO
D. 4Fe(OH) 2 + O2 + 2H2 O → 4Fe(OH) 3
Hướng dẫn giải
Nx: Đáp án A và B không có sự thay đổi số oxi hóa nên không phải là phản ứng oxi hóa khử. Còn lại đáp án C và D.
Phản ứng hóa hợp là phản ứng từ nhiều chất tham gia tạo thành 1 chất mới. Do đó loại đáp án C.
⇒ Chọn D
2.2. Dạng 2: Cách xác định chất khử, chất oxi hóa trong phản ứng hóa học
Bài 1: Cho phản ứng: Ca + Cl2 → CaCl2 .
Kết luận nào sau đây đúng?
A. Mỗi nguyên tử Ca nhận 2e.
B. Mỗi nguyên tử Cl nhận 2e.
C. Mỗi phân tử Cl2 nhường 2e.
D. Mỗi nguyên tử Ca nhường 2e.
Hướng dẫn giải
Ca → Ca2++2e
Cl2 + 2.1e → 2Cl-
⇒ Chọn D
Bài 2: Trong phản ứng: CaCO3 → CaO + CO2 , nguyên tố cacbon
A. Chỉ bị oxi hóa.
B. Chỉ bị khử.
C. Vừa bị oxi hóa, vừa bị khử.
D. Không bị oxi hóa, cũng không bị khử.
Hướng dẫn giải
C+4 → C+4
⇒ Chọn D
Bài 3: Trong phản ứng: Cu + 2H2SO4(đặc, nóng) → CuSO4 + SO2 + 2H2 O, axit sunfuric
A. là chất oxi hóa.
B. vừa là chất oxi hóa, vừa là chất tạo môi trường.
C. là chất khử.
D. vừa là chất khử, vừa là chất tạo môi trường.
Hướng dẫn giải
S+6 → S+4 ⇒ H2SO4 đóng vai trò là chất oxi hóa
Mặt khác SO42- đóng vai trò môi trường để tao muối CuSO4
⇒ Chọn B
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Đốt cháy hoàn toàn 4,8g bột than trog không khí. Thể tích khí thu được sau phản ứng là?
Câu 2: Cần điều chế 33,6 g sắt bằng cách dùng khí co khử Fe3O4.
a. Viết phương trình hoá học.
b. Tính khối lượng Fe3O4 cần dùng.
c. Tính thể tích khí CO (đktc) đã dùng.
Câu 3: Dẫn luồng khí H2 dư đi qua 16 g hỗn hợp hai oxit CuO và Fe2O3 nung nóng. Sau phản ứng để nguội, cân lại thấy khối lượng hỗn hợp giảm 25%. Tính phần trăm khối lượng của mỗi oxit trong hỗn hợp đầu.
Câu 4: Người ta dùng khí cacbon oxit để khử đồng(II) oxit.
a. Nếu khử a gam đồng(II) oxit thì thu được bao nhiêu gam đồng?
b. Cho a = 150 g, hãy tính kết quả bằng số.
3.2. Bài tập trắc nghiệm
Câu 1: Chọn đáp án đúng
A. Sự tách Oxi khỏi hợp chất được gọi là sự oxi hóa
B. Sự tác dụng của oxi với một chất gọi là sự khử
C. Chất khử là chất chiếm oxi của chất khác
D. Chất oxi hóa là chất chiếm oxi của chất khác
Câu 2: Cho phản ứng sau, xác định chất khử
Fe2O3 + 3H2 −to→ 2Fe + 3H2O
A. Fe2O3
B. H2
C. Fe
D. H2O
Câu 3: Oxit nào bị khử bởi Hidro:
A. Na2O
B. CaO
C. Fe3O4
D. BaO
Câu 4: Cho phản ứng:
3Fe + 2O2 −to→ Fe3O4
Chất nào là chất khử?
A. Fe
B. O2
C.Fe3O4
D.Cả A & B
Câu 5: Phản ứng nào không phải phản ứng oxi hóa – khử:
A. 4Na + O2 −to→ 2Na2O
B. Cl2 + 2KBr → 2KCl + Br2
C. NH3 + HCl → NH4Cl
D. 2NaOH + Cl2 → NaCl + NaClO + H2O
4. Kết luận
Sau bài học cần nắm:
- Phân biệt chất khử, chất oxi hóa, sự khử, sự oxi hóa trong những phản ứng oxi hóa – khử cụ thể
- Phân biệt phản ứng oxi hóa – khử với các loại phản ứng khác.
Tham khảo thêm
- doc Hoá học 8 Bài 31: Tính chất - Ứng dụng của hiđro
- doc Hoá học 8 Bài 33: Điều chế khí hiđro - Phản ứng thế
- doc Hoá học 8 Bài 34: Bài luyện tập 6
- doc Hoá học 8 Bài 35: Bài thực hành 5
- doc Hoá học 8 Bài 36: Nước
- doc Hoá học 8 Bài 37: Axit Bazơ Muối
- doc Hoá học 8 Bài 38: Bài luyện tập 7
- doc Hoá học 8 Bài 39: Bài thực hành 6



