Giải bài tập SGK Hóa 9 Bài 4: Một số axit quan trọng
Hướng dẫn Giải bài tập Hóa học 9 Bài 4 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 19 SGK Hóa 9
Có những chất: CuO, BaCl2, Zn, ZnO. Chất nào nói trên tác dụng với dung dịch HCl và dung dịch H2SO4 loãng, sinh ra:
a) Chất khí cháy được trong không khí?
b) Dung dịch có màu xanh lam?
c) Chất kết tủa màu trắng không tan trong nước và axit?
d) Dung dịch không màu và nước?
Viết tất cả các phương trình phản ứng.
Phương pháp giải
a) Chất khí cháy được trong không khí → sinh ra khí H2
b) Dung dịch có màu xanh lam là dung dịch muối đồng (II)
c) Chất kết tủa trắng không tan trong nước và axit là BaSO4
d) Dung dịch không màu là muối kẽm
Hướng dẫn giải
Câu a: Khí cháy được trong không khí là hiđro
Zn + 2HCl → ZnCl2 + H2
Zn + H2SO4 → ZnSO4 + H2
Câu b: Dung dịch có màu xanh lam là dung dịch muối đồng (II)
CuO + 2HCl → CuCl2 + H2O
CuO + H2SO4 → CuSO4 + H2O
Câu c: Chất kết tủa trắng không tan trong nước và axit là BaSO4
BaCl2 + H2SO4 → 2HCl + BaSO4
Câu d: Dung dịch không màu là muối kẽm
ZnO + 2HCl → ZnCl2 + H2O
ZnO + H2SO4 → ZnSO4 + H2O
2. Giải bài 2 trang 19 SGK Hóa 9
Sản xuất axit sunfuric trong công nghiệp cần phải có những nguyên liệu chủ yếu nào? Hãy cho biết mục đích của mỗi công đoạn sản xuất axit sunfuric và dẫn ra những phản ứng hóa học.
Phương pháp giải
Để xác định mục đích các công đoạn sản xuất axit sunfuric cần nắm được lý thuyết về sản xuất axit sunfuric.
Hướng dẫn giải
- Sản xuất axit sunfuric trong công nghiệp cần phải có nguyên liệu là lưu huỳnh (hoặc quặng pirit), không khí và nước.
- Mục đích của mỗi công đoạn sản xuất axit sunfuric:
- Đốt lưu huỳnh trong không khí để sản xuất lưu huỳnh đioxit:
S + O2 → SO2
- Oxi hóa SO2 (V2O5) để sản xuất SO3:
2SO2 + O2 2SO3
- Cho SO3 tác dụng với H2O để sản xuất H2SO4:
SO3 + H2O → H2SO4
3. Giải bài 3 trang 19 SGK Hóa 9
Bằng cách nào có thể nhận biết từng chất trong mỗi cặp chất sau theo phương pháp hóa học:
a) Dung dịch HCl và dung dịch H2SO4.
b) Dung dịch NaCl và dung dịch Na2SO4.
c) Dung dịch Na2SO4 và dung dịch H2SO4.
Viết các phương trình phản ứng.
Phương pháp giải
Phương pháp hóa học nhận biết trong mỗi trường hợp như sau:
a) Dùng muối Ba2+ như BaCl2; Ba(NO3)2 hoặc Ba(OH)2
b) Tương tự ý a
c) Dùng quỳ tím hoặc dùng kim loại như Mg, Al, Zn, Fe...
Hướng dẫn giải
Câu a: Nhận biết dung dịch HCl và dung dịch H2SO4
Lấy mỗi dung dịch một ít làm mẫu thử
Cho dung dịch BaCl2 vào hai ống nghiệm có chứa dung dịch HCl và dung dịch H2SO4:
- Chất trong ống nghiệm nào cho kết tủa màu trắng, suy ra chất ban đầu là H2SO4.
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
- Chất trong ống nghiệm không có hiện tượng gì xảy ra là HCl.
Câu b: Nhận biết dung dịch NaCl và dung dịch Na2SO4
Lấy mỗi dung dịch một ít làm mẫu thử
Dùng một trong những thuốc thử sau: BaCl2, Ba(NO3)2, dung dịch Ba(OH)2
- Chất nào cho kết tủa màu trắng, suy ra chất ban đầu là Na2SO4.
BaCl2 + Na2SO4 → BaSO4↓ + 2NaCl
- Chất không có hiện tượng gì xảy ra là NaCl.
Câu c: Nhận biết dung dịch Na2SO4 và dung dịch H2SO4
Cho giấy quỳ tím vào hai ống nghiệm chứa Na2SO4 và H2SO4:
- Chất nào làm quỳ tím đổi màu thành đỏ là dung dịch H2SO4.
- Còn chất không làm quỳ tím đổi màu là Na2SO4.
4. Giải bài 4 trang 19 SGK Hóa 9
Bảng dưới đây cho biết kết quả của 6 thí nghiệm xảy ra giữa Fe và dung dịch H2SO4 loãng. Trong mỗi thí nghiệm người ta dùng 0,2 gam Fe tác dụng với thể tích bằng nhau của axit, nhưng có nồng độ khác nhau.
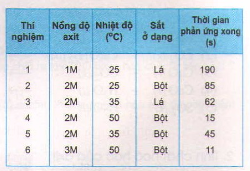
Những thí nghiệm nào chứng tỏ rằng:
a) Phản ứng xảy ra nhanh hơn khi tăng nhiệt độ?
b) Phản ứng xảy ra nhanh hơn khi tăng diện tích tiếp xúc?
c) Phản ứng xảy ra nhanh hơn khi tăng nồng độ axit?
Phương pháp giải
Để xác định thí nghiệm nào xảy ra nhanh hơn ở mỗi trường hợp ta cần giữ nguyên các điều kiện còn lại và chỉ có sự thay đổi điều kiện đó.
Hướng dẫn giải
So sánh các điều kiện: nồng độ axit, nhiệt độ của dung dịch H2SO4 loãng và trạng thái của sắt với thời gian phản ứng để rút ra:
a) Thí nghiệm 2, thí nghiệm 4 và thí nghiệm 5 chứng tỏ phản ứng xảy ra nhanh hơn khi tăng nhiệt độ của dung dịch H2SO4 .
b) Thí nghiệm 3 và thí nghiệm 5 chứng tỏ phản ứng xảy ra nhanh hơn khi tăng diện tích tiếp xúc.
c) Thí nghiệm 4 và thí nghiệm 6 chứng tỏ phản ứng xảy ra nhanh hơn khi tăng nồng độ của dung dịch H2SO4.
5. Giải bài 5 trang 19 SGK Hóa 9
Hãy sử dụng những chất có sẵn: Cu, Fe, CuO, KOH, C6H12O6 (glucozơ), dung dịch H2SO4 loãng, H2SO4 đặc và những dụng cụ thí nghiệm cần thiết để làm những thí nghiệm chứng minh rằng:
a) Dung dịch H2SO4 loãng có những tính chất chung của axit.
b) H2SO4 đặc có những tính chất hóa học riêng.
Viết phương trình hóa học cho mỗi thí nghiệm.
Phương pháp giải
Để chứng minh tính chất của H2SO4 loãng và H2SO4 đặc cần nắm tính chất hóa học đặc trưng:
a) Chứng minh tính chất của H2SO4 loãng:
- Tác dụng với oxit bazơ.
- Tác dụng với bazơ.
- Tác dụng với kim loại đứng trước H trong dãy điện hóa.
b) H2SO4 đặc có những tính chất hóa học riêng: tính oxi hóa mạnh; tính háo nước.
Hướng dẫn giải
Câu a: Để chứng minh dung dịch H2SO4 loãng có những tính chất hóa học của axit, ta thực hiện các thí nghiệm:
Cho axit H2SO4 loãng lần lượt phản ứng với Fe, CuO, KOH:
- H2SO4 + Fe → FeSO4 + H2↑ (có khí thoát ra)
- H2SO4 + CuO → CuSO4 + H2O (dung dịch có màu xanh lam)
- H2SO4 + 2KOH → K2SO4 + 2H2O (Cho quỳ tím vào dung dịch KOH, dung dịch có màu xanh. Rót từ từ dung dịch H2SO4 thấy màu xanh dần biến mất đến khi dung dịch không màu)
Câu b: Để chứng minh dung dịch H2SO4 đặc có những tính chất hóa học riêng ta thực hiện các thí nghiệm:
Cho axit H2SO4 đặc tác dụng với Cu đun nóng và với glucozơ:
- 2H2SO4(đặc, nóng) + Cu → CuSO4 + SO2 + 2H2O
(Đồng bị hòa tan dần, dung dịch chuyển sang màu xanh và có khí mùi hắc thoát ra)
- C6H12O6 → 6H2O + 6C (xt: H2SO4 đặc)
(Đường bị hóa thành than và đẩy lên khỏi cốc)
6. Giải bài 6 trang 19 SGK Hóa 9
Cho một khối lượng mạt sắt dư vào 50ml dung dịch HCl. Phản ứng xong thu được 3,36 lít khí (đktc).
a) Viết phương trình hóa học.
b) Tính khối lượng mạt sắt đã tham gia phản ứng.
c) Tính nồng độ mol của dung dịch HCl đã dùng.
Phương pháp giải
a) Phương trình hóa học: Fe + 2HCl → FeCl2 + H2
b) Dựa vào phương trình, tính được mol Fe phản ứng theo số mol của H2
Đổi số mol H2: nH2 = 3,36/22,4 = ? (mol)
nFe = nH2 → Khối lượng sắt
c) Công thức tính nồng độ mol CM = n : V
Hướng dẫn giải
Câu a: Phương trình hóa học
Fe + 2HCl → FeCl2 + H2 ↑
Câu b: Số mol khí H2 = 3,36:22,4 = 0,15 mol
Phương trình hóa học:
Fe + 2HCl → FeCl2 + H2 ↑
0,15 0,3 0,15 ← 0,15 (mol)
Khối lượng sắt đã phản ứng:
mFe = 0,15.56 = 8,4 (g).
Câu c: Số mol HCl phản ứng
nHCl = 0,3 mol; 50 ml = 0,05 lít
Nồng độ mol của dung dịch HCl: CM,HCl = 0,3 / 0,05 = 6M.
7. Giải bài 7 trang 19 SGK Hóa 9
Hòa tan hoàn toàn 12,1g hỗn hợp bột CuO và ZnO cần 100ml dung dịch HCl 3M.
a) Viết các phương trình hóa học.
b) Tính phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu.
c) Hãy tính khối lượng dung dịch H2SO4 có nồng độ 20 % để hòa tan hoàn toàn hỗn hợp các oxit trên.
Phương pháp giải
Để giải quyết các dữ kiện của đề bài, ta thực hiện các bước sau:
- Bước 1: Gọi x, y là số mol của CuO và ZnO, viết phương trình hóa học:
CuO + 2HCl → CuCl2 + H2O
ZnO + 2HCl → ZnCl2 + H2O
y → 2y y (mol)
- Bước 3: Giải hệ 2 ẩn 2 phương trình theo khối lượng hỗn hợp và số mol HCl.
- Bước 4: Vì CuO và ZnO phản ứng với H2SO4 theo cùng tỉ lệ mol, nên có thể coi hai oxit như một oxit có công thức chung là MO với số mol = x + y = 0,15 mol
MO + H2SO4 → MSO4 + H2O
Dựa vào phương trình, tính được số mol H2SO4 → khối lượng dung dịch H2SO4.
Hướng dẫn giải
Câu a: Phương trình hóa học xảy ra
CuO + 2HCl → CuCl2 + H2O (1)
ZnO + 2HCl → ZnCl2 + H2O (2)
Câu b: Phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu
nHCl = 0,3 mol
Đặt x và y lần lượt là số mol CuO và ZnO trong hỗn hợp
Dựa vào phương trình trên ta có:
nHCl = 2nCuO = 2x; nHCl = 2nZnO = 2y
→ 2x + 2y = 0,3
Kết hợp dữ kiện đề bài cho ta có hệ phương trình:
\(\left\{ {\begin{array}{*{20}{l}}
{2x + 2y = 0,3}\\
{80x + 81y = 12,1}
\end{array}} \right. \Rightarrow \left\{ {\begin{array}{*{20}{l}}
{x = 0,05}\\
{y = 0,1}
\end{array}} \right.\)
Phần trăm theo khối lượng của mỗi oxit trong hỗn hợp ban đầu là:
\(\\ \%m_{CuO }= \frac{0,05 . 80 . 100\%}{ 12,1 }= 33 \ \% \\ và \\ \%m_{ZnO} = 100 \% - 33 \% = 67 \ \%\)
Câu c: Khối lượng dung dịch H2SO4 có nồng độ 20 % để hòa tan hoàn toàn hỗn hợp các oxit trên
Khối lượng H2SO4 cần dùng:
mH2SO4 = 98.(x + y) = 98.(0,05 + 0,1) = 14,7 (g).
Khối lượng dung dịch H2SO4 20% cần dùng:
\(m_{H_{2}SO_{4}} = \frac{14,7 .100 }{20} = 73,5 \ g\)
Tham khảo thêm
- docx Giải bài tập SGK Hóa 9 Bài 1: Tính chất HH của oxit và Khái quát về sự PL oxit
- docx Giải bài tập SGK Hóa 9 Bài 2: Một số oxit quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 3: Tính chất hóa học của axit
- docx Giải bài tập SGK Hóa 9 Bài 5: Luyện tập TCHH của oxit và axit
- docx Giải bài tập SGK Hóa 9 Bài 7: Tính chất hóa học của bazơ
- docx Giải bài tập SGK Hóa 9 Bài 8: Một số bazơ quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 9: Tính chất hóa học của muối
- docx Giải bài tập SGK Hóa 9 Bài 10: Một số muối quan trọng
- docx Giải bài tập SGK Hóa 9 Bài 11: Phân bón hóa học
- docx Giải bài tập SGK Hóa 9 Bài 12: Mối quan hệ giữa các loại hợp chất vô cơ
- docx Giải bài tập SGK Hóa 9 Bài 13: Luyện tập chương 1 Các loại hợp chất vô cơ



