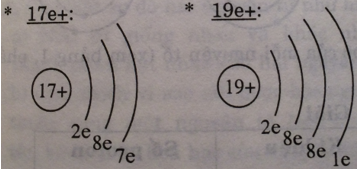Giải bài tập SBT Hóa 8 Bài 4: Nguyên tử
Hướng dẫn Giải bài tập Sách bài tập Hóa học 8 Bài 4 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về nguyên tử. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 4.1 trang 4 SBT Hóa học 8
Điền tên hạt nào tạo thành nguyên tử vào các câu sau đây (chép vào ở bài tập):
a) ... và ... có điện tích như nhau, chỉ khác dấu.
b) …. và …. có cùng khối lượng, còn …. có khối lượng rất bé, không đáng kể.
c) Những nguyên tử cùng loại có cùng số …. trong hạt nhân.
d) Trong nguyên tử ... luôn chuyển động rất nhanh và sắp xếp thành từng lớp.
Phương pháp giải
Để trả lời các câu hỏi trên cần nắm rõ lý thuyết về nguyên tử.
Hướng dẫn giải
a) Proton và electron;
b) Proton và nơtron, electron;
c) Proton;
d) Các electron.
2. Giải bài 4.2 trang 5 SBT Hóa học 8
Có thể dùng các cụm từ sau đây để nói về nguyên tử:
A. Vô cùng nhỏ.
B. Trung hòa về điện.
C. Tạo ra các chất.
D. Không chia nhỏ hơn trong phản ứng hóa học.
Hãy chọn cụm từ phù hợp (A, B, C hay D?) với phần còn lại trống trong câu:
"Nguyên tử là hạt ..., vì số electron có trong nguyên tử bằng đúng số proton trong hạt nhân".
Phương pháp giải
Vì mỗi electron mang điện tích (-), mỗi proton mang điện tích (+) nên về số trị: tổng điện tích âm bằng tổng điện tích dương.
Hướng dẫn giải
"Nguyên tử là hạt trung hòa về điện, vì số electron có trong nguyên tử bằng đúng số proton trong hạt nhân".
Đáp án B.
3. Giải bài 4.3 trang 5 SBT Hóa học 8
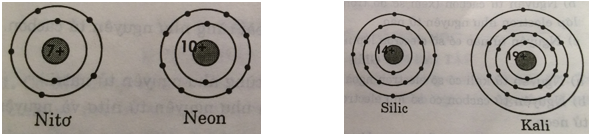
Cho biết sơ đồ một số nguyên tử sau:
Hãy chỉ ra số proton trong hạt nhân, số electron trong nguyên tử, số lớp electron và số electron lớp ngoài cùng của mỗi nguyên tử.
Phương pháp giải
Cần dựa vào lý thuyết về nguyên tử và sơ đồ của nguyên tử được cho ở trên để xác định số proton trong hạt nhân, số electron trong nguyên tử, số lớp electron và số electron lớp ngoài cùng của mỗi nguyên tử.
Hướng dẫn giải
- Nitơ:
+ Số p trong hạt nhân: 7
+ Số e trong nguyên tử: 7
+ Số lớp electron: 2
+ Số e lớp ngoài cùng: 5
- Neon:
+ Số p trong hạt nhân: 10
+ Số e trong nguyên tử: 10
+ Số lớp electron: 2
+ Số e lớp ngoài cùng: 8
- Silic:
+ Số p trong hạt nhân: 14
+ Số e trong nguyên tử: 14
+ Số lớp electron: 3
+ Số e lớp ngoài cùng: 4
- Kali:
+ Số p trong hạt nhân: 19
+ Số e trong nguyên tử: 19
+ Số lớp electron: 4
+ Số e lớp ngoài cùng: 1
4. Giải bài 4.4 trang 5 SBT Hóa học 8
Theo sơ đồ một số nguyên tử ở bài tập 4.3, hãy chỉ ra:
a) Mỗi nguyên tử có mấy lớp electron.
b) Những nguyên tử nào có cùng một số lớp electron.
c) Nguyên tử nào có số lớp electron như nguyên tử natri. (xem sơ đồ trong Bài 4 - SGK).
Phương pháp giải
a) 1 vòng tròn tượng trưng 1 lớp e
b) Nguyên tử có cùng lớp e sẽ có cùng số vòng tròn
c) Số lớp e của nguyên tử Silic = Số lớp e của nguyên tử Natri = 3
Hướng dẫn giải
a) Nitơ → 2 lớp electron
Neon → 2 lớp electron
Silic → 3 lớp electron
Kali → 4 lớp electron
b) Nguyên tử có cùng số electron: nitơ, neon.
c) Nguyên tử sillic có cùng số lớp electron như nguyên tử natri. (3 lớp e)
5. Giải bài 4.5 trang 5 SBT Hóa học 8
Yêu cầu như bài 4.4.
a) Nguyên tử nào có số electron lớp ngoài cùng như nguyên tử natri.
b) Nguyên tử cacbon (xem sơ đồ trong bài tập 5, bài 4 – SGK) có số lớp electron như nguyên tử nào.
c) Nguyên tử nào có số electron lớp ngoài cùng như nguyên tử cacbon.
Phương pháp giải
+) 1 chấm đen tượng trưng cho 1 e => Số chấm đen ở vòng tròn ngoài cùng là số e lớp ngoài cùng của nguyên tử
+) Các nguyên tử có cùng số lớp e sẽ có cùng số vòng tròn
Hướng dẫn giải
a) Nguyên tử kali có số electron ngoài cùng như nguyên tử natri. (1 e lớp ngoài cùng)
b) Nguyên tử cacbon có số lớp electron như nguyên tử nitơ và nguyên tử neon. (2 lớp e)
c) Nguyên tử sillic có số electron có số electron lớp ngoài cùng như nguyên tử cacbon. (4 e lớp ngoài cùng)
6. Giải bài 4.6 trang 6 SBT Hóa học 8
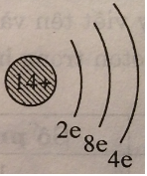
Có thể vẽ sơ đồ đơn giản gồm vòng tròn con là hạt nhân, mỗi vòng cung nhỏ là một lớp với số electron của lớp ghi ở chân. Thí dụ sơ đồ đơn giản của nguyên tử sillic trong bài tập 4.3 như sau:
Biết rằng, trong nguyên tử các electron có ở lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4.
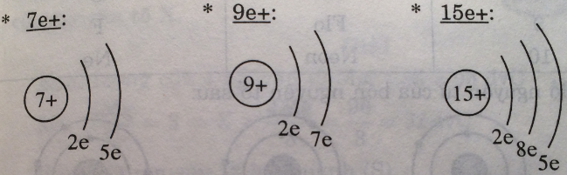
a) Vẽ sơ đồ đơn giản của năm nguyên tử mà trong hạt nhân có số proton bằng 7, 9, 15, 17, 19.
b) Mấy nguyên tử có số electron ở lớp ngoài cùng bằng 5, mấy nguyên tử có số electron ở lớp ngoài cùng bằng 7 ?
Phương pháp giải
a) Cách vẽ giản đồ
- Bước 1: Vẽ 1 vòng tròn đậm trong cùng có ghi điện tích của hạt nhân nguyên tử.
- Bước 2: Lần lượt vẽ các vòng tròn tiếp theo (mỗi vòng tròn tượng trưng 1 lớp e).
- Bước 3: Điền số e tương ứng trên các vòng tròn (chú ý lớp 1 (tính từ hạt nhân) tối đa là 2e, ở lớp 2 tối đa là 8e, ở lớp 3 tạm thời cũng là 8e, nếu còn electron sẽ ở lớp 4).
b) Số e trên vòng tròn ngoài cùng (tính từ hạt nhân) chính là số e lớp ngoài cùng của nguyên tử.
Hướng dẫn giải
a) Nguyên tử có hạt nhân có số proton lần lượt là 7e+; 9e+; 15e+; 17e+; 19e+.
b) - Hai nguyên tử có số eletron lớp ngoài cùng là 5.
- Hai nguyên tử có số electron ngoài cùng 7.
Tham khảo thêm
- doc Giải bài tập SBT Hóa 8 Bài 2: Chất
- doc Giải bài tập SBT Hóa 8 Bài 5: Nguyên tố hóa học
- doc Giải bài tập SBT Hóa 8 Bài 6: Đơn chất- Hợp chất- Phân tử
- doc Giải bài tập SBT Hóa 8 Bài 8: Luyện tập
- doc Giải bài tập SBT Hóa 8 Bài 9: Công thức hóa học
- doc Giải bài tập SBT Hóa 8 Bài 10: Hóa trị
- doc Giải bài tập SBT Hóa 8 Bài 11: Luyện tập chương 1