Giải bài tập SGK Hóa 11 Bài 40: Ancol
Để giúp các em học sinh học tập thật tốt bộ môn Hóa học 11, eLib xin giới thiệu nội dung giải bài tập SGK bên dưới đây. Tài liệu gồm tất cả các bài tập có phương pháp và hướng dẫn giải chi tiết, rõ ràng, sẽ giúp các em ôn tập lại kiến thức, cũng cố kĩ năng làm bài hiệu quả. Mời các em cùng tham khảo.
Mục lục nội dung
1. Giải bài 1 trang 186 SGK Hóa học 11
2. Giải bài 2 trang 186 SGK Hóa học 11
3. Giải bài 3 trang 186 SGK Hóa học 11
4. Giải bài 4 trang 186 SGK Hóa học 11
5. Giải bài 5 trang 187 SGK Hóa học 11
6. Giải bài 6 trang 187 SGK Hóa học 11
7. Giải bài 7 trang 187 SGK Hóa học 11

1. Giải bài 1 trang 186 SGK Hóa học 11
Viết công thức cấu tạo và gọi tên các ancol đồng phân của nhau có công thức phân tử C5H12O
Phương pháp giải
Ancol có 2 loại đồng phân:
+ Đồng phân về mạch C ( mạch nhánh và mạch không phân nhánh)
+ Đồng phân về vị trí nhóm chức
Hướng dẫn giải
Công thức cấu tạo và tên gọi các ancol đồng phân có công thức phân tử C5H12O
CH3-CH2-CH2-CH2-CH2OH: pentan -1 –ol
CH3-CH2-CH2-CH(OH)-CH3: Pentan-2-ol
CH3-CH2-CH(OH)-CH2-CH3: pentan-3-ol
CH3-CH(CH3)-CH2-CH2OH: 3-metylbutan-1-ol
CH3-CH(CH3)-CH(OH)-CH3: 3-metylbutan-2-ol
CH3-(OH)C(CH3)-CH2-CH3: 2-metylbutan-2-ol
CH3-CH2-CH(CH3)-CH2OH: 2-metylbutan-1-ol
CH3-C(CH3)2-CH2OH: 2,2-ddimetylpropan-1-ol
2. Giải bài 2 trang 186 SGK Hóa học 11
Viết các phương trình hóa học của phản ứng giữa propan-1-ol với mỗi chất sau:
a) Natri kim loại
b) CuO, đun nóng
c) Axit HBr, có xúc tác.
Trong mỗi phản ứng trên, ancol đóng vai trò gì: chất khử, chất oxi hóa, axit, bazơ ?
Phương pháp giải
a) phản ứng với Na là phản ứng thế nguyên tử H trong nhóm OH bằng nguyên tử KL Na
b) ancol bậc 1 phản ứng với CuO, đun nóng sẽ tách nước tạo thành anđehit
c) ancol phản ứng với HBr là phản ứng thế cả nhóm -OH bằng nguyên tử Br
Ghi nhớ: chất khử là chất nhường e, số oxi hóa tăng sau phản ứng
chất oxi hóa là chất nhận electron, số oxi hóa giảm sau phản ứng
axit là chất nhường proton( tức cho H+)
Bazơ là chất nhận proton ( tức nhận H+ )
Hướng dẫn giải
a. 2CH3-CH2-CH2OH + 2Na → 2CH3-CH2-CH2ONa + H2
Ancol là Chất oxi hóa (vì là chất nhận electron, số oxi hóa giảm sau phản ứng)
b. CH3-CH2-CH2OH + CuO → CH3-CH2-CHO + Cu + H2O
Ancol là Chất khử (vì là chất nhường electron, số oxi hóa tăng sau phản ứng)
c. CH3-CH2-CH2OH + HBr → CH3-CH2-CH2Br + H2O
Ancol là Bazơ (vì nhận H+ của HBr)
3. Giải bài 3 trang 186 SGK Hóa học 11
Trình bày phương pháp hóa học để phân biệt các chất lỏng đựng riêng biệt trong các lọ không dán nhãn: etanol, glixerol, nước và benzen.
Phương pháp giải
Dựa vào độ tan của các chất trong nước và tính chất hóa học đặc trưng của các chất để phân biệt.
Hướng dẫn giải
Trích mỗi chất 1 ít cho ra các ống nghiệm khác nhau và đánh số thứ tự tương ứng.
- Cho lần lượt nước dư vào các ống nghiệm:
+ ống nghiệm nào chất lỏng không tan, dung dịch phân thành 2 lớp là benzen ( nổi lên trên bề mặt nước)
+ các ống nghiệm còn lại dung dịch đồng nhất là: etanol (C2H5OH), glixerol ( C3H5(OH)3), nước (H2O)
- Cho Cu(OH)2 vào 3 chất còn lại, chất nào tạo phức màu xanh lam là C3H5(OH)3, còn lại không có hiện tượng gì là C2H5OH và H2O
2C3H5(OH)3 + Cu(OH)2 → [C3H5(OH)2O]2Cu + 2H2O
Đốt 2 chất còn lại, rồi cho sản phẩm qua dung dịch nước vôi trong, chất nào sản phẩm sinh ra làm đục nước vôi trong là C2H5OH, còn lại là H2O
C2H5OH + 3O2 → 2CO2 + 3H2O
CO2 + Ca(OH)2 → CaCO3↓ + H2O
4. Giải bài 4 trang 186 SGK Hóa học 11
Từ propen và các chất vô cơ cần thiết có thể điều chế được các chất sau đây: propan-2-ol (1); propan-1,2-điol (2). Viết phương trình hóa học của các phản ứng xảy ra.
Phương pháp giải
Có thể viết phương trình theo sơ đồ sau:
CH3CH=CH2 (+ HBr) → CH3CHBrCH3 (+NaOH) → CH3CH(OH)CH3
CH3CH=CH2 (+Br2) → CH3CHBrCH2Br (+NaOH) → CH3CH(OH)CH2OH
Hướng dẫn giải
Điều chế propan-2-ol, propan-1,2-điol từ propen
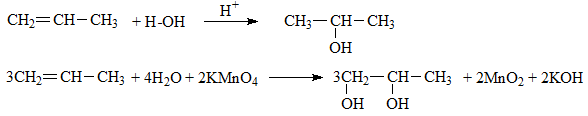
5. Giải bài 5 trang 187 SGK Hóa học 11
Cho 12,20 g hỗn hợp X gồm etanol và propan -1 –ol tác dụng với natri (dư) thu được 2,80 lít khí (đktc).
a) Tính thành phần phần trăm khối lượng của mỗi chất trong hỗn hợp X
b) Cho hỗn hợp X qua ống đựng CuO đun nóng. Viết phương trình hóa học của phản ứng.
Phương pháp giải
a) \({n_{{H_2}}} = \frac{{2,8}}{{22,4}} = 0,125{\mkern 1mu} mol\)
Gọi số mol của C2H5OH và CH3CH2CH2OH lần lượt là x và y (mol)
C2H5OH + Na → C2H5ONa + ½ H2↑
x 0,5x (mol)
CH3CH2CH2OH + Na → CH3CH2CH2ONa + ½ H2↑
y 0,5y (mol)
Giải hệ phương trình:
\(\begin{array}{l} \sum {{m_{ancol}} = 46x + 60y = 12,2} \\ \sum {{n_{{H_2}}} = 0,5x + 0,5y = 0,125} \\ \to x = ?y = ? \end{array}\)
→ %C2H5OH và CH3CH2CH2OH
b) Ghi nhớ: oxi hóa ancol bậc 1 bằng CuO nung nóng sản phẩm tạo thành gồm anđehit, Cu và H2O
Hướng dẫn giải
a) \({n_{{H_2}}} = \frac{{2,8}}{{22,4}} = 0,125{\mkern 1mu} (mol)\)
Gọi số mol của C2H5OH và CH3CH2CH2OH lần lượt là x và y (mol)
C2H5OH + Na → C2H5ONa + ½ H2↑
x 0,5x (mol)
CH3CH2CH2OH + Na → CH3CH2CH2ONa + ½ H2↑
y 0,5y (mol)
Giải hệ phương trình:
\(\begin{array}{l} \left\{ \begin{array}{l} \sum {{m_{ancol}} = 46x + 60y = 12,2} \\ \sum {{n_{{H_2}}} = 0,5x + 0,5y = 0,125} \end{array} \right. \to \left\{ \begin{array}{l} x = 0,2\\ y = 0,05 \end{array} \right.\\ \to \% {C_2}{H_5}OH = \frac{{{m_{{C_2}{H_5}OH}}}}{{{m_{hh{\kern 1pt} ancol}}}}.100\% = \frac{{0,2.46}}{{12,2}}.100\% = 75,4\% \\ \% C{H_3}C{H_2}C{H_2}OH = 100\% - 75,4\% = 25,60\% \end{array}\)
b) C2H5OH + CuO → CH3CHO + Cu↓ + H2O
CH3CH2CH2OH + CuO → C2H5CHO + Cu↓ + H2O
6. Giải bài 6 trang 187 SGK Hóa học 11
Oxi hóa hoàn toàn 0,60 g một ancol A đơn chức bằng oxi không khí, sau đó dẫn sản phẩm qua bình (1) đựng H2SO4 đặc rồi dẫn tiếp qua bình (2) đựng dung dịch KOH. Khối lượng bình (1) tăng 0,72g; bình (2) tăng 1,32 g.
a) Giải thích hiện tượng thí nghiệm trên bằng các phương trình hóa học.
b) Tìm công thức phân tử, viết công thức cấu tạo có thể có của A
c) Khi cho ancol trên tác dụng với CuO, đun nóng thu được một anđêhit tương ứng. Gọi tên của A.
Phương pháp giải
a) Đốt cháy ancol sinh ra sản phẩm gồm H2O và CO2
H2SO4 đặc có tính háo nước nên sản phẩm bình (1) tăng là khối lượng của H2O
dung dịch KOH hấp thụ khí CO2 nên sản phẩm bình (2) tăng là khối lượng của CO2
b) Tính số mol H2O, số mol CO2
Bảo toàn khối lượng → mO( trong A) = mA – mC - mH
Gọi CTPT của ancol A đơn chức là CxHyO
Có: nA = nO( trong A)
\(\begin{array}{l} \to x = \frac{{{n_{C{O_2}}}}}{{{n_A}}} = ?\\ y = \frac{{2{n_{{H_2}O}}}}{{{n_A}}} = ? \end{array}\)
→ CTPT của A từ đó viết được CTCT của A
c) ancol A tác dụng với CuO, đun nóng thu được anđehit → ancol A phải là ancol bậc 1 => từ đó tìm được CTCT chính xác của A
Hướng dẫn giải
a) Sản phẩm oxi hóa gồm CO2 và H2O đi qua bình (1) đựng H2SO4 đặc thì H2O bị hấp thụ làm bình (1) tăng mH2O = 0,72 (g) ; qua bình (2) CO2 bị hấp thụ bởi dung dịch KOH, mCO2 = 1,32 (g).
2CxHyO + \(\frac{{4x + y - 2}}{2}\) O2 → 2xCO2 + yH2O
CO2 + 2KOH → K2CO3 + H2O
b) \({n_{{H_2}O}} = \frac{{0,72}}{{18}} = 0,04{\mkern 1mu} (mol)\)
\({n_{C{O_2}}} = \frac{{1,32}}{{44}} = 0,03{\mkern 1mu} (mol)\)
Bảo toàn khối lượng: mO(trong A) = mA – mC - mH
→ mO (trong A) = 0,6 – 0,03.12 – 0,04.2= 0,16 (g)
→ nO = 0,16/16 = 0,01 (mol)
Gọi CTPT của ancol A đơn chức là CxHyO : 0,01 (mol) ( Vì ancol đơn chức nên nA = nO)
\(\begin{array}{l} x = \frac{{{n_{C{O_2}}}}}{{{n_A}}} = \frac{{0,03}}{{0,01}} = 3\\ y = \frac{{2{n_{{H_2}O}}}}{{{n_A}}} = \frac{{0,08}}{{0,01}} = 8 \end{array}\)
Vậy CTPT của A là: C3H8O
CTCT có thể có của A là: CH3CH2CH2 OH; CH3CH(OH)CH3
c) A + CuO nung nóng → anđehit
→ A là ancol bậc 1
→ CTCT của A là CH3CH2CH2OH: propan-1-ol
CH3CH2CH2OH + CuO → CH3CH2CHO + Cu↓+ H2O
7. Giải bài 7 trang 187 SGK Hóa học 11
Từ 1,00 tấn tinh bột có chứa 5,0% chất xơ (không bị biến đổi) có thể sản xuất được bao nhiêu lít etanol tinh khiết, biết hiệu suất chung của cả quá trình sản xuất là 80,0% và khối lượng riêng của etanol D = 0,789 g/ml
Phương pháp giải
Viết phương trình hóa học xảy ra, tính toán số mol C2H5OH theo số mol của tinh bột
(C6H10O5)n + nH2O → nC6H12O6 (1)
C6H12O6 → 2C2H5OH + 2CO2 (2)
Ghi nhớ công thức:
mrượu = V.D
\(\% H = \frac{{luong{\mkern 1mu} thuc{\mkern 1mu} te}}{{luong{\mkern 1mu} li{\mkern 1mu} thuyet}}.100\% \)
Hướng dẫn giải
Khối lượng chất xơ là: mxơ = \(\frac{{{{10}^6}.5\% }}{{100\% }} = 0,{05.10^6}{\mkern 1mu} (g)\)
Khối lượng tinh bột là: mtb = 106 - 0,05.106 = 0,95.106 (g)
(C6H10O5)n + nH2O → nC6H12O6 (1)
C6H12O6 → 2C2H5OH + 2CO2 (2)
Từ (1) và (2) ta có:
\(\begin{array}{l} {n_{{C_2}{H_5}OH}} = 2{n_{{C_6}{H_{12}}{O_6}}} = 2n.{n_{{C_6}{H_{10}}{O_5}}} = 2n.\frac{{0,{{95.10}^6}}}{{162n}} = \frac{{1,{{9.10}^6}}}{{162}}\\ \to {m_{{C_2}{H_5}OH}} = \frac{{1,{{9.10}^6}}}{{162}}.46 = \frac{{87,{{4.10}^6}}}{{162}}(g)\\ \to {V_{{C_2}{H_5}OH}} = \frac{m}{D} = \frac{{87,4.106}}{{162.0,789}}(ml) \end{array}\)
Vì %H = 80% nên lượng ancol thực tế thu được là:
\({V_{{C_2}{H_5}OH}}tt = \frac{{87,{{4.10}^6}}}{{162.0,789}}.\frac{{80\% }}{{100\% }} = 0,{547.10^6}(ml) = 547{\mkern 1mu} (l)\)
8. Giải bài 8 trang 187 SGK Hóa học 11
Tên nào dưới đây ứng với ancol trên?
CH3-CH(CH3)-CH2-CH2-CH2OH
A. 2-metylpentan-1-ol
B. 4-metylpentan-1-ol
C. 4-metylpentan-2-ol
D. 3-metylhexan-2-ol
Phương pháp giải
Quy tắc đọc tên:
+ Chọn mạch cacbon dài nhất, chứa nhiều nhánh nhất làm mạch chính
+ Đánh chỉ số từ phía gần nhóm -OH hơn
Tên ancol = tên số chỉ vị trí nhánh + tên nhánh + tên mạch cacbon chính + số chỉ vị trí nhóm -OH +ol
Hướng dẫn giải
Đánh số thứ tự từ cacbon gần nhóm chức -OH nhất
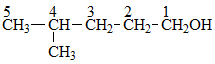
Nhóm -OH ở cacbon số 1 là: 1-ol
Nhánh metyl ở cacbon số 4 là: 4-metyl
⇒ Tên ứng với ancol là 4-metylpentan-1-ol
⇒ Đáp án đúng là B
9. Giải bài 9 trang 187 SGK Hóa học 11
Cho 3,70 gam một ancol X no,đơn chức, mạch hở tác dụng với natri dư thấy có 0,56 lít khí thoát ra (đktc). Công thức phân tử của X là:
A. C2H6O
B. C3H10O
C. C4H10O
D. C4H8O
Phương pháp giải
Đổi số mol H2 = ?
Gọi công thức của ancol X no đơn chức, mạch hở là CnH2n+1OH ( n≥ 1)
PTHH: 2CnH2n+1OH + 2Na → 2CnH2n+1ONa + H2↑
nC2H5OH = 2nH2 = ?
→ MC2H5OH = m : nC2H5OH → n =? → CTPT của X
Hướng dẫn giải
Số mol hiđro sinh ra là:
\({n_{{H_2}}} = \frac{{0,56}}{{22,4}} = 0,025(mol)\)
Phương trình hóa học:
2CnH2n+1OH + 2Na → 2CnH2n+1ONa + H2↑
0,05 0,025
\(\begin{array}{l}
{M_{ROH}} = \frac{{3,7}}{{0,05}} = 74(g/mol)\\
\Rightarrow {M_R} = 74 - 17 = 57\\
\Rightarrow 14n + 1 = 57 \Rightarrow n = 4
\end{array}\)
Công thức phân tử của X là C4H10O
⇒ Chọn C
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Bài 39: Dẫn xuất halogen của hiđrocacbon
- doc Giải bài tập SGK Hóa 11 Bài 41: Phenol
- doc Giải bài tập SGK Hóa 11 Bài 42: Luyện tập Dẫn xuất halogen, ancol, phenol



