Hoá học 10 Bài 9: Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học và Định luật tuần hoàn
Nội dung bài học Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học và Định luật tuần hoàn tìm hiểu Thế nào là tính kim loại, tính phi kim của các nguyên tố hóa học? Sự biến đổi tuần hoàn tính kim loại, tính phi kim? Khái niệm độ âm điện và sự biến đổi tuần hoàn độ âm điện. Sự biến đổi tuần hoàn hóa trị cao nhất đối với oxi của nguyên tố trong oxit và hóa trị cao nhất trong hợp chất khí đối với hiđro. Sự biến đổi tính chất oxit và hiđroxit của các nguyên tố nhóm A. Hiểu được định luật tuần hoàn.
Mục lục nội dung

1. Tóm tắt lý thuyết
1.1. Tính kim loại, tính phi kim
- Kim loại là những nguyên tố dễ mất electron để trở thành ion dương
- Phi kim là những nguyên tố dễ nhận electron để trở thành ion âm.
- Kim loại càng mạnh khi khả năng mất electron càng lớn.
- Phi kim càng mạnh khi khả năng nhận electron càng lớn.
a. Sự biến đổi tính chất trong một chu kì
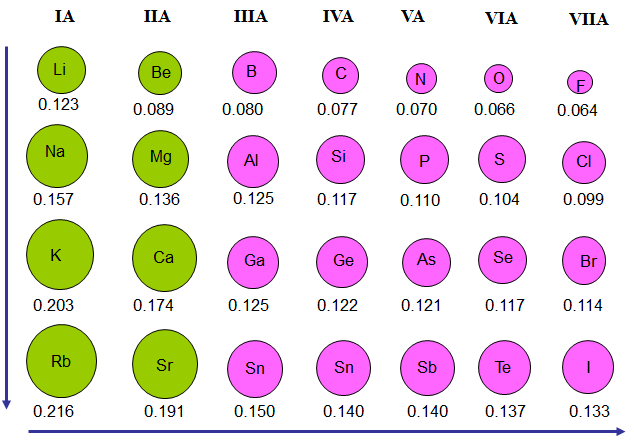
- Trong mỗi chu kì, bán kính nguyên tử giảm từ trái qua phải
- Trong mỗi nhóm A, bán kính nguyên tử tăng từ trên xuống dưới
- Trong chu kì tính kim loại giảm dần, tính phi kim tăng dần.
- Theo chiều tăng dần của điện tích hạt nhân thì điện tích hạt nhân tăng dần, số lớp electron không đổi, lực hút giữa hạt nhân và electron lớp ngoài cùng tăng, làm cho bán kính nguyên tử giảm khả năng mất electron giảm, khả năng nhận electron tăng.
b. Sự biến đổi tính chất trong một nhóm A
- Tính kim loại tăng dần, tính phi kim giảm dần.
- Theo chiều tăng dần của điện tích hạt nhân trong nhóm A, số lớp electron tăng dần, làm cho bán kính nguyên tử tăng, lực hút giữa hạt nhân và electron lớp ngoài cùng giảm, khả năng mất electron tăng, khả năng nhận electron giảm.
- Trong nhóm A theo chiều tăng dần của điện tích hạt nhân, tính kim loại của các nguyên tố tăng dần đồng thời tính phi kim giảm dần.
c. Độ âm điện
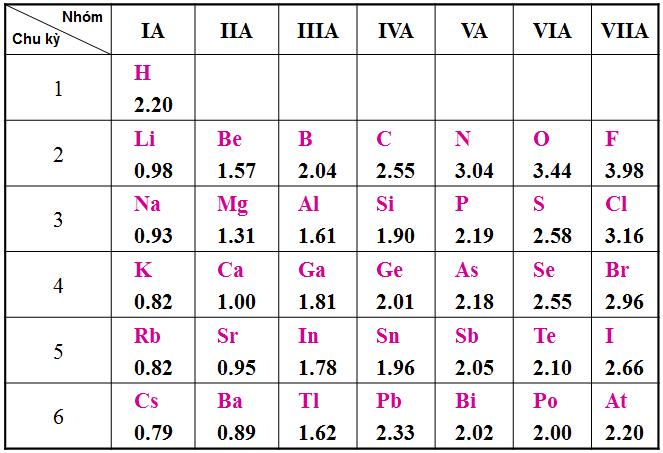
- Độ âm điện của một nguyên tử càng lớn thì tính phi kim của nó càng mạnh và ngược lại.
- Trong chu kì theo chiều tăng dần của điện tích hạt nhân giá trị độ âm điện tăng dần.
- Trong nhóm A theo chiều tăng dần của diện tích hạt nhân, giá trị độ âm điện giảm dần.
- Sự biến đổi giá trị độ âm điện và tính kim loại, tính phi kim phù hợp với nhau.
- Độ âm điện của một nguyên tố càng lớn thì tính phi kim càng mạnh, tính kim loại càng giảm và ngược lại.
1.2. Hóa trị của các nguyên tố
- Trong chu kì 3 đi từ đi từ trái sang phải, hóa trị cao nhất của các nguyên tố đối với oxi tăng từ 1 đến 7 còn hóa trị trong hợp chất khí đối với hiđro giảm từ 4 đến 1
- Trong chu kì hóa trị cao nhất của các nguyên tố đối với oxi tăng dần và hiđro giảm dần.
Nhóm IA:
+ Hợp chất với Oxi: R2O
+ Hóa trị cao nhất với Oxi: 1
Nhóm IIA:
+ Hợp chất với Oxi: RO
+ Hóa trị cao nhất với Oxi: 2
Nhóm IIIA:
+ Hợp chất với Oxi: R2O3
+ Hóa trị cao nhất với Oxi: 3
Nhóm IVA:
+ Hợp chất với Oxi: RO2
+ Hợp chất với Hidro: RH4
+ Hóa trị cao nhất với Oxi: 4
+ Hóa trị với Hidro: 4
Nhóm VA:
+ Hợp chất với Oxi: R2O5
+ Hợp chất với Hidro: RH3
+ Hóa trị cao nhất với Oxi: 5
+ Hóa trị với Hidro: 3
Nhóm VIA:
+ Hợp chất với Oxi: RO3
+ Hợp chất với Hidro: R2S
+ Hóa trị cao nhất với Oxi: 6
+ Hóa trị với Hidro: 2
Nhóm VIIA:
+ Hợp chất với Oxi: R2O7
+ Hợp chất với Hidro: HX
+ Hóa trị cao nhất với Oxi: 7
+ Hóa trị với Hidro: 1
1.3. Oxit và hiđroxit của các nguyên tố nhóm A
Tính bazơ của các oxit và hiđroxit giảm dần đồng thời tính axit của nó mạnh dần.
Na2O + H2O → 2NaOH
Cl2O7 + H2O ⇔ 2HClO4
1.4. Định luật tuần hoàn
Tính chất của các nguyên tố và đơn chất cũng như thành phần và tính chất của các hợp chất tạo nên từ các nguyên tố đó biến đổi tuần hoàn theo chiều tăng dần của điện tích hạt nhân nguyên tử.
2. Bài tập minh họa
2.1. Dạng 1: Sự biến thiên tính chất của các nguyên tố hóa học
Bài 1. Dãy các nguyên tố nào dưới đây được sắp xếp theo chiều tăng dần tính kim loại?
A. Li, Be, Na, K.
B. Al, Na, K, Ca.
C. Mg, K, Rb, Cs.
D. Mg, Na, Rb, Sr.
Hướng dẫn giải
Trong 1 chu kì, tính kim loại giảm dần (đi từ trái qua phải).
Trong 1 nhóm, tính kim loại tăng dần (đi từ trên xuống dưới).
Do đó dãy sắp xếp tăng dần tính kim loại là: Mg, K, Rb, Cs
⇒ Chọn C
Bài 2. Cho các nguyên tố X, Y, Z với số hiệu nguyên tử lần lượt là 4, 12, 20. Phát biểu nào sau đây sai?
A. Các nguyên tố này đều là các kim loại mạnh nhất trong chu kì.
B. Các nguyên tố này không cùng thuộc 1 chu kì.
C. Thứ tự tăng dần tính bazo là: X(OH)2, Y(OH) 2, Z(OH) 2
D. Thứ tự tăng dần độ âm điện là: Z < Y < X
Hướng dẫn giải
Zx= 4 ⇒ cấu hình e lớp ngoài cùng của X là … 2s2 ⇒ X thuộc nhóm II, chu kì 2
Zy = 12 ⇒ cấu hình e lớp ngoài cùng của Y là ….3s2 ⇒ Y thuộc nhóm II, chu kì 3
Zz = 20 ⇒ cấu hình e lớp ngoài cùng của Z là ….4s2⇒ Z thuộc nhóm II, chu kì 4
A sai vì nguyên tố nhóm IA mới là KL mạnh nhất trong 1 CK
B đúng X thuộc CK 2, Y thuộc CK 3, Z thuộc CK 4.
C đúng Trong cùng 1 nhóm tính bazo tăng dần theo chiều tăng dần của điện tích hạ nhân.
D đúng Trong cùng 1 nhóm độ âm điện giảm dần theo chiều tăng dần của điện tích hạt nhân.
⇒ Chọn A
2.2. Dạng 2: Cách xác định nguyên tố thuộc 2 nhóm A liên tiếp trong Bảng HTTH
Bài 1. A và B là hai nguyên tố ở cùng một nhóm và thuộc hai chu kì liên tiếp trong bảng tuần hoàn. Tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32. Hãy viết cấu hình electron của A, B và của các ion mà A và B có thể tạo thành.
Hướng dẫn giải
Theo bài ra, tổng số proton trong hai hạt nhân nguyên tử của A và B bằng 32 nên ZA + ZB = 32.
Trường hợp 1: ZB - ZA = 8. Ta tìm được ZA = 12; ZB = 20.
Cấu hình electron:
A : 1s22s22p63s2 (chu kỳ 3, nhóm IIA).
và B: 1s22s22p63s23p64s2 (chu kỳ 4, nhóm IIA).
Ion A2+: 1s22s22p6 và B2+: 1s22s22p63s23p6.
Trường hợp 2: ZB - ZA = 18. Ta tìm được ZA = 7; D = 25.
Cấu hình electron:
A : 1s22s22p3 (chu kỳ 2, nhóm VA).
và B: 1s22s22p63s23p63d54s2 (chu kỳ 4, nhóm VIIB).
Trường hợp này A, B không cùng nhóm nên không thỏa mãn.
Bài 2. Cho 8,8 gam một hỗn hợp hai kim loại nằm ở hai chu kì liên tiếp nhau và thuộc nhóm IIIA, tác dụng với HCl dư thì thu được 6,72 lít khí hidro (đktc). Dựa vào bảng tuần hoàn cho biết tên hai kim loại đó.
Hướng dẫn giải
Kí hiệu hai kim loại nhóm IIIA là M, nguyên tử khối trung bình là M−
Phương trình hóa học có dạng: 2M + HCl → 2MCl2 + 3H2
nH2 = 6,72/22,4 = 0,3 (mol)
nM = 2/3 nH2 = 0,2 (mol)
theo đầu bài: M− .0,2 = 8,8 → M− = 44
hai kim loại thuộc hai chu kì liên tiếp, một kim loại có nguyên tử khối nhỏ hơn 44 và một kim loại có nguyên tử khối lơn hơn 44.
Dựa vào bảng tuần hoàn, hai kim loại đó là:
Al (M = 27 < 44) và Ga (M = 69,72 > 44).
2.3. Dạng 3: Xác định hai nguyên tố thuộc cùng 1 nhóm A
X và Y là hai nguyên tố trong cùng một nhóm A và ở hai chu kì liên tiếp của bảng tuần hoàn. Tổng số proton trong hạt nhân của hai nguyên tử X và Y bằng 30. Cấu hình electron của X là (biết MX < MY)
A. 1s22s22p63s23p64s1
B. 1s22s22p2
C. 1s22s22p63s1
D. [Ar]3d54s1
Hướng dẫn giải
Vì X và Y thuộc cùng một nhóm A và ở chu kì liên tiếp nên ta có:
\(\left[ \begin{array}{l}
\left\{ \begin{array}{l}
{Z_X} + {Z_Y} = 30\\
{Z_Y} - {Z_X} = 8
\end{array} \right.\\
\left\{ \begin{array}{l}
{Z_X} + {Z_Y} = 30\\
{Z_Y} - {Z_X} = 18
\end{array} \right.
\end{array} \right. \to \left[ \begin{array}{l}
\left\{ \begin{array}{l}
{Z_X} = 11(Na)\\
{Z_Y} = 19(K)
\end{array} \right.\\
\left\{ \begin{array}{l}
{Z_X} = 6(C)\\
{Z_Y} = 24(Cr)
\end{array} \right.
\end{array} \right.\)
X và Y là hai nguyên tố trong cùng một nhóm A ⇒ X là Na và Y là K
Khi đó cấu hình electron là của Na là 1s22s22p63s1
⇒ Đáp án C
2.4. Dạng 4: Cách xác định nguyên tố thông qua nguyên tử khối
Bài 1. Cho 10 gam kim loại A (thuộc nhóm IIA) tác dụng với nước, thu được 6,11 lit khí hiđro (đo ở 25oC và 1 atm).
a. Hãy xác định tên của kim loại M đã dùng.
b. Cho 4 gam kim loại A vào cốc đựng 2,5lit dung dịch HCl 0,06M thu được dung dịch B.
Hướng dẫn giải
A + 2H2O → A(OH)2 + H2
a a
Số mol khí H2 = 0,25 (mol) ⇒ a = 0,25
Ta có: MA = 10/0,25 = 40 (Ca).
b. Số mol Ca = 4/40 = 0,1 mol. Các phương trình phản ứng:
Ca + 2HCl → CaCl2 + H2
0,075 0,15 0,075
Ca + 2H2O → Ca(OH)2 + H2
0,025 0,025
Dung dịch B gồm: CaCl2 = 0,075 mol và Ca(OH)2 = 0,025 mol.
3. Luyện tập
3.1. Bài tập tự luận
Câu 1: Hợp cất khí của nguyên tố R với hidro có công thức hóa học RH4. Trong oxit mà R có hóa trị cao nhất, R chiếm 46,67% về khối lượng. Nguyên tố R thuộc chu kì
Câu 2: Đại lượng đặc trưng cho khả năng hút electron của nguyên tử các nguyên tố khi hình thành liên kết hoá học là
Câu 3: Bán kính nguyên tử của các nguyên tố: 3Li, 8O, 9F, 11Na được xếp theo thứ tự tăng dần từ trái sang phải là
Câu 4: X, Y là hai kim loại có electron cuối cùng là 3p1 và 3d6.
a. Dựa vào bảng tuần hoàn, hãy xác định tên hai kim loại X, Y.
b. Hòa tan hết 8,3 gam hỗn hợp X, Y vào dung dịch HCl 0,5M (vừa đủ), ta thấy khối lượng dung dịch sau phản ứng tăng thêm 7,8 gam. Tính khối lượng mỗi kim loại và thể tích dung dịch HCl đã dùng.
3.2. Bài tập trắc nghiệm
Câu 1: Trong một chu kì, theo chiều tang dần của điện tích hạt nhân,
A. bán kính nguyên tử giảm dần, tính kim loại tăng dần.
B. bán kính nguyên tử giảm dần, tính phi kim tăng dần.
C. bán kính nguyên tử tăng dần, tính phi kim tăng dần.
D. bán kính nguyên tử tăng dần, tính phi kim giảm dần.
Câu 2: Dãy nguyên tố nào sau đây được sắp xếp theo chiều tang dần độ âm điện?
A. Li, Na, C, O, F
B. Na, Li, F, C, O
C. Na, Li, C, O, F
D. Li, Na, F, C, O
Câu 3: Dãy nguyên tố nào sau đây được sắp xếp theo chiều tang dần tính kim loại?
A. Li, Be, Na, K
B. Al, Na, K, Ca
C. Mg, K, Rb, Cs
D. Mg, Na, Rb, Sr
Câu 4: Cho các nguyên tố X, Y, Z với sô hiệu nguyên tử lần lượt là 4, 12, 20. Phát biểu nào sau đây là sai?
A. Các nguyên tố này đều là kim loại mạnh nhất trong chu kì.
B. Các nguyên tố này không cùng thuộc một chu kì.
C. Thứ tự tăng dần tính bazơ la X(OH)2 < Y(OH)2 < Z(OH)2.
D. Thứ tự tang dần độ âm điện: X < Y < Z.
Câu 5: Cho các nguyên tố X, Y, Z với số hiệu nguyên tử lần lượt là 11, 29, 37. Phát biểu nào sau đây đúng?
A. Các nguyên tố này đều là kim loại nhóm IA.
B. Các nguyên tố này không cùng một chu kì.
C. Thứ tự tính kim loại tang dần: X < Y < Z.
D. Thứ tự tính bazơ tang dần: XOH < YOH < ZOH.
3.3. Trắc nghiệm Online
Các em hãy luyện tập bài trắc nghiệm Sự biến đổi tuần hoàn tính chất của các nguyên tố hóa học và Định luật tuần hoàn Hóa học 10 sau để nắm rõ thêm kiến thức bài học.
4. Kết luận
Sau bài học cần nắm:
- Thế nào là tính kim loại, tính phi kim của các nguyên tố hóa học?
- Sự biến đổi tuần hoàn tính kim loại, tính phi kim? Khái niệm độ âm điện và sự biến đổi tuần hoàn độ âm điện.
- Sự biến đổi tuần hoàn hóa trị cao nhất đối với oxi của nguyên tố trong oxit và hóa trị cao nhất trong hợp chất khí đối với hiđro.
- Sự biến đổi tính chất oxit và hiđroxit của các nguyên tố nhóm A.
- Hiểu được định luật tuần hoàn.
Tham khảo thêm
- doc Hoá học 10 Bài 7: Bảng tuần hoàn các nguyên tố hóa học
- doc Hoá học 10 Bài 8: Sự biến đổi tuần hoàn cấu hình electron nguyên tử của các nguyên tố hóa học
- doc Hoá học 10 Bài 10: Ý nghĩa của bảng tuần hoàn các nguyên tố hóa học
- doc Hoá học 10 Bài 11: Luyện tập Bảng tuần hoàn, sự biến đổi tuần hoàn cấu hình electron nguyên tử và tính chất của các nguyên tố hóa học



