Giải bài tập SBT Hóa 12 Bài 1: Este
Hướng dẫn Giải bài tập Sách bài tập Hóa học 12 Bài 1 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về tính chất của este. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 1.1 trang 3 SBT Hóa học 12
2. Giải bài 1.2 trang 3 SBT Hóa học 12
3. Giải bài 1.3 trang 3 SBT Hóa học 12
4. Giải bài 1.4 trang 3 SBT Hóa học 12
5. Giải bài 1.5 trang 4 SBT Hóa học 12
6. Giải bài 1.6 trang 4 SBT Hóa học 12
7. Giải bài 1.7 trang 4 SBT Hóa học 12
8. Giải bài 1.8 trang 4 SBT Hóa học 12
9. Giải bài 1.9 trang 4 SBT Hóa học 12
10. Giải bài 1.10 trang 5 SBT Hóa học 12
11. Giải bài 1.11 trang 5 SBT Hóa học 12

1. Giải bài 1.1 trang 3 SBT Hóa học 12
Ứng với công thức phân tử (CTPT) C4H8O2 có bao nhiêu este đồng phân của nhau ?
A. 2. B. 3. C.4. D. 5
Phương pháp giải
- Bước 1: Tính k (tổng số liên kết π và vòng trong phân tử), tìm số liên kết π trong gốc hiđrocacbon.
- Bước 2: Viết các đồng phân của este fomat HCOOR’ (R’ mạch không nhánh, có nhánh).
- Bước 3: Thực hiện chuyển lần lượt 1 cacbon từ gốc R’ sang gốc R cho đến khi R’ chỉ còn H thì dừng lại.
Hướng dẫn giải
k = 1
- Vì este đơn chức có một liên kết trong nhóm COO nên gốc R và R' đều là gốc hiđrocacbon no.
Các đồng phân của este fomat HCOOR'
1. HCOOCH2CH2CH3
2. HCOOCH(CH3)2
- Chuyển lần lượt 1C từ gốc R' sang gốc R
3. CH3COOC2H5
4. C2H5COOCH3
Ta thấy ở đồng phân thứ 4, R' chỉ còn 1C nên đã là đồng phân cuối cùng.
Vậy CTPT C4H8O2 có 4 đồng phân este
→ Chọn C.
2. Giải bài 1.2 trang 3 SBT Hóa học 12
Cho các chất có công thức cấu tạo sau đây :
(1) CH3CH2COOCH3; (2) CH3OOCCH3 ; (3) HCOOC2H5 ; (4)CH3COOH;
(5) 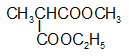
(7) CH3OOC-COOC2H5
Những chất thuộc loại este là
A. (1),(2), (3), (4), (5), (6).
B. (1), (2), (3), (5), (7).
C. (1), (2), (4), (6), (7).
D.(1), (2), (3), (6), (7).
Phương pháp giải
Dựa vào định nghĩa về este: Khi ta thay thể nhóm (-OH) trong phân tử axit bằng gốc (-OR') thì thu được este.
Chú ý: Cách viết khác của este
R - COO - R' hoặc R' - OOC - R hoặc R' - OCO - R (R'≠ H)
Hướng dẫn giải
Các chất (1), (2), (3), (5), (7) thuộc loại este.
→ Chọn B.
3. Giải bài 1.3 trang 3 SBT Hóa học 12
Hợp chất X đơn chức có công thức đơn giản nhất là CH2O. X tác dụng được với dung dịch NaOH nhưng không tác dụng được với natri. Công thức cấu tạo của X là
A. CH3COOH. B. CH3COOCH3.
C. HCOOCH3 D. OHCCH2OH.
Phương pháp giải
X tác dụng được với dung dịch NaOH nhưng không tác dụng được với Na, suy ra X là este.
Hướng dẫn giải
X tác dụng được với dung dịch NaOH nhưng không tác dụng với Na X là este.
Dựa vào đáp án X có 2 nguyên tử O trong phân tử
CTPT của X là C2H4O2 CTCT của X là HCOOCH3
→ Chọn C.
4. Giải bài 1.4 trang 3 SBT Hóa học 12
Hợp chất X có công thức cấu tạo: CH3OOCCH2CH3. Tên gọi của X là
A. etyl axetat. B. metyl propionat
C. metyl axetat. D. propyl axetat.
Phương pháp giải
Danh pháp của este RCOOR' = tên gốc hiđrocacbon R' + tên gốc axit ("ic" "at").
Hướng dẫn giải
CH3OOCCH2CH3 = CH3CH2COOCH3
Gốc -CH3: metyl
Axit CH3CH2COOH : axit propionic
Vậy este CH3CH2COOCH3 có tên là metyl propionat.
→ Chọn B.
5. Giải bài 1.5 trang 3 SBT Hóa học 12
Thuỷ phân este E có công thức phân tử C4H8O2 (có mặt H2SO4 loãng) thu được 2 sản phẩm hữu cơ X và Y. Từ X có thể điều chế trực tiếp ra Y bằng một phản ứng duy nhất. Tên gọi của E là
A. metyl propionat. B. propyl fomat.
C. ancol etylic. D. etylaxetat.
Phương pháp giải
- Dựa vào công thức ở mỗi đáp án, viết phương trình hóa học.
- Từ sản phẩm tạp thành xét xem sản phẩm thủy phân có thể điều chế trực tiếp ra chất còn lại hay không để chọn đáp án đúng.
Hướng dẫn giải
Đáp án A: \({C_2}{H_5}{\text{COOC}}{{\text{H}}_3} + {H_2}O\xrightarrow{{{H_2}S{O_4}}}{C_2}{H_5}{\text{COO}}H + C{H_3}OH\)
Sản phẩm thủy phân không thể điều chế trực tiếp ra chất còn lại.
Đáp án B: \(HCOO{C_3}{H_7} + {H_2}O\xrightarrow{{{H_2}S{O_4}}}HCOOH + {C_3}{H_7}OH\)
Sản phẩm thủy phân không thể điều chế trực tiếp ra chất còn lại.
Đáp án C: ancol etylic không bị thủy phân
Đáp án D: \(C{H_3}{\text{COO}}{{\text{C}}_2}{H_5} + {H_2}O\xrightarrow{{{H_2}S{O_4}}}C{H_3}{\text{COO}}H + {C_2}{H_5}OH\)
\({C_2}{H_5}OH + {O_2}\xrightarrow{{xt,{t^o}}}C{H_3}{\text{COO}}H + {H_2}O\)
Chọn đáp án D.
6. Giải bài 1.6 trang 3 SBT Hóa học 12
Thuỷ phân hoàn toàn 3,7 gam este X có công thức phân tử C3H602 trong 100 g dung dịch NaOH 4%, cô cạn dung dịch sau phản ứng thu được 5,4 g chất rắn. Công thức cấu tạo của X là
A. HCOOC2H5 B. HCOOC3H7
C. CH3COOCH3 D. CH3COOC2H5
Phương pháp giải
- Bảo toàn khối lượng tìm khối lượng ancol.
- Vì X là este đơn chức nên nancol = nX Mancol
Công thức cấu tạo của X
Hướng dẫn giải
= 3,7/74 = 0,05 mol
= (100.4)/100=4 gam
Bảo toàn khối lượng:
mX + mNaOH = mrắn + mancol
→ 3,7 + 4 = 5,4 + mancol
→mancol = 2,3 gam
Vì X là este đơn chức nên nancol = nX = 0,05 mol
= 2,3/0,05 =46
→Ancol: C2H5OH
C2H5
→ Chọn A.
7. Giải bài 1.7 trang 4 SBT Hóa học 12
Thuỷ phân hoàn toàn hỗn hợp gồm hai este đơn chức X. Y là đồng phân cấu tạo của nhau cần 100 ml dung dịch NaOH 1M. Thu được 7.85 g hỗn hợp hai muối của hai axit là đồng đẳng kế tiếp và 4.95g 2 hai ancol bậc I. Công thức cấu tạo và phần trăm khối lượng của hai este là :
A. HCOOCH2CH2CH3, 75% ; CH3COOC2H5, 25%.
B. HCOOC2H5, 45% ; CH3COOCH3, 55%.
C. HCOOC2H5, 55% ; CH3COOCH3, 45%.
D. HCOOCH2CH2CH3, 25% ; CH3COOC2H5, 75%.
Phương pháp giải
Bảo toàn khối lượng để tìm khối lượng hỗn hợp este
- Vì este là đơn chức nên neste = nNaOH
CTPT của X và Y CTCT của X, Y.
- Đặt số mol của X và Y lần lượt là x, y mol.
- Lập hệ phương trình, suy ra phần trăm khối lượng của hai este
Hướng dẫn giải
nNaOH = 0,1.1 = 0,1 mol
Theo định luật bảo toàn khối lượng, ta có:
mhh este = mmuối + mrượu – mNaOH = 7,85 + 4,95 – 0,1.40 = 8,8 g
Theo đề bài hỗn hợp este là đơn chức → nNaOH = nhh este = 0,1 mol
→ Meste = 88 g/mol.
Dựa vào đáp án, hh este là hh este no, đơn chức→Công thức phân tử của 2 este là C4H8O2
→ Loại đáp án B, C
→ Hỗn hợp este gồm HCOOC3H7 (x mol) và CH3COOC2H5 (y mol).
Từ phản ứng thuỷ phân và khối lượng sản phẩm muối ta có hệ pt
H7 + nCH3COOC2H5 = x + y = 0,1
a + mCH3COONa = 67x + 82y = 7,85
→ x = 0,025 mol; y = 0,075 mol
→ %H7 = 25% ; %COOC2H5 = 75%
→ Chọn D.
8. Giải bài 1.8 trang 4 SBT Hóa học 12
Este X có công thức đơn giản nhất là C2H4O. Đun sôi 4,4 g X với 200 g dung dịch NaOH 3% đến khi phản ứng xảy ra hoàn toàn. Từ dung dịch sau phản ứng thu được 8,1 g chất rắn khan. Công thức cấu tạo của X là
A.CH3CH2COOCH3. B. CH3COOCH2CH3
C. HCOOCH2CH2CH3. D. HCOOCH(CH3)2.
Phương pháp giải
- Từ đáp án suy ra CTPT của X → số mol của X
- Vì nX < nNaOH → chất rắn gồm muối và NaOH dư → khối lượng của muối
- nX = nmuối → CT của muối
→ Công thức este.
Hướng dẫn giải
= (200.3)/(100.40) =0,15 mol
Từ đáp án → Công thức phân tử của X là C4H8O2.
→ nX = 0,05 mol. Đặt CTHH của X dạng RCOOR’
PT: RCOOR’ + NaOH → RCOONa + R’OH
nX = nNaOH (pư) = 0,05 mol
→ mNaOH(dư) = 0,1 mol
→ Chất rắn thu được gồm RCOONa 0,05 mol và NaOH dư 0,1 mol
mRCOONa = mchất rắn – mNaOH(dư) = 4,1 g → MRCOONa = 82 → MR = 15
→ CTCT của X là CH3COOC2H5
→ Chọn B.
9. Giải bài 1.9 trang 4 SBT Hóa học 12
Đồng phân nào trong số các đồng phân mạch hở có công thức phân tử C2H4O2 tác dụng được với
a) Dung dịch natri hiđroxit ?
b) Natri kim loại ?
c) Ancol etylic ?
d) Dung dịch AgNO3/NH3 sinh ra Ag ?
Viết các phương trình hoá học minh hoạ.
Phương pháp giải
- Viết các đồng phân cấu tạo của CTPT C2H4O2
- Dựa vào tính chất hóa học của các chất tương ứng.
Hướng dẫn giải
Ứng với công thức phân tử C2H4O2 có các công thức cấu tạo mạch hở sau: CH3COOH (A); HCOOCH3 (B); HOCH2CHO (C).
Tác dụng được với dung dịch natri hiđroxit : A và B.
CH3COOH + NaOH → CH3COONa + H2O
HCOOCH3 + NaOH → HCOONa + CH3OH
Tác dụng được với natri kim loại : A và C.
CH3COOH + Na → CH3COONa + ½ H2
HOCH2CHO + Na → NaOCH2CHO + ½ H2
Tác dụng được với ancol etylic : A và C.
C2H5OH + CH3COOH \(\xrightarrow{{{H^ + },{t^o}}}\) CH3COOC2H5 + H2O
C2H5OH + HOCH2CHO → C2H5OCH2CHO + H2O
Tác dụng được với AgNO3/NH3 sinh ra Ag : B và C.
HCOOCH3 + 2AgNO3 + 2NH3 → NH4OOCOCH3 + 2Ag + NH4NO3 + H2O
HOCH2CHO + 2AgNO3 + 2NH3 → HOCH2COONH4 + 2Ag + NH4NO3 + H2O
10. Giải bài 1.10 trang 5 SBT Hóa học 12
Este đơn chức X có phần trăm khối lượng các nguyên tố C, H, O lần lượt là 48,65% ; 8,11% và 43,24%
a) Tìm công thức phân tử, viết các công thức cấu tạo có thể có và gọi tên X.
b) Đun nóng 3,7 g X với dung dịch NaOH vừa đủ đến khi phản ứng xảy ra hoàn toàn. Từ dung dịch sau phản ứng, thu được 4,1 g muối rắn khan. Xác định công thức cấu tạo của X.
Phương pháp giải
a. Từ phần trăm khối lượng các nguyên tố, ta xác định được công thức đơn giản nhất của X là C3H6O2 → Công thức phân tử của X là C3H6O2.
Viết các đồng phân ứng với CTPT đã tìm được, dựa vào lý thuyết về danh pháp của este và gọi tên các este tương ứng.
b. Gọi công thức của X là RCOOR1 (R1 # H)
Muối khan là RCOONa có số mol = số mol X
Công thức của muối
Công thức của este.
Hướng dẫn giải
a. Gọi CTPT của X là CxHyOz
x : y : z = (48,65/12) : (8,11/1) : (43,24/16) = 3: 6 : 2
Công thức đơn giản nhất của X là C3H6O2
Vì X là este đơn chức → Công thức phân tử của X là C3H6O2
Các công thức cấu tạo có thể có của X là :
HCOOC2H5 (etyl fomat) và CH3COOCH3 (metyl axetat).
b. Đặt công thức của X là RCOOR1 (R1 # H).
RCOOR1 + NaOH → RCOONa + R1OH
nX = 0,05 mol
Muối khan là RCOONa có số mol = số mol X = 0,05 mol
=> M RCOONa= = 82 (g/mol)
Từ đó suy ra muối là CH3COONa.
Công thức cấu tạo của X là CH3COOCH3
11. Giải bài 1.11 trang 5 SBT Hóa học 12
Hai este X và Y là đồng phân cấu tạo của nhau. Tỉ khối hơi của X so với hiđro bằng 44.
a) Tìm công thức phân tử của X và Y.
b) Cho 4,4 g hồn hợp X và Y tác dụng với dung dịch NaOH vừa đủ đến khi các phản ứng xảy ra hoàn toàn, thu được 4,45 g chất rắn khan và hỗn hợp hai ancol là đồng đẳng kế tiếp. Xác định công thức cấu tạo của X, Y và gọi tên chúng.
Phương pháp giải
a. Từ tỷ khối hơi của X so với hiđro, tìm được MX
Công thức phân tử của X, Y.
b. Vì X, Y đều đơn chức nên neste = nmuối
Công thức của 2 muối
Công thức cấu tạo của X, Y.
Hướng dẫn giải
a) MX = 44.2 = 88 (g/mol).
Vì nhóm COO trong phân tử este có khối lượng là 44, nên X và Y thuộc loại este đơn chức dạng RCOOR' hay CxHyO2.
Ta có : 12x + y = 56 → x = 4;y = 8
Công thức phân tử của X và Y là C4H8O2. X, Y thuộc loại este no, đơn chức, mạch hở.
b) Đặt công thức chung của 2 este là RCOOR ’. Phản ứng thủy phân trong dung dịch NaOH:
RCOOR’ + NaOH → RCOONa + R’OH
Chất rắn khan là hỗn hợp muối của hai axit là đồng đẳng kế tiếp (vì hai ancol là đồng đẳng kế tiếp).
neste = nmuối = = 0,05 mol
M RCOONa = = 89 (g\mol)
→ R = 22.
Hai muối tương ứng là CH3COONa và C2H5COONa.
X là CH3COOCH2CH3 (etyl axetat), Y là C2H5COOCH3 (metyl propionat).
12. Giải bài 1.12 trang 5 SBT Hóa học 12
Este đơn chức X thu được từ phản ứng este hoá giữa ancol Y và axit hữu cơ Z (có xúc tác là axit H2SO4). Đốt cháy hoàn toàn 4,3 g X thu được 4,48 lít khí CO2 (đktc) và 2,7 g nước. Tìm công thức phân tử, viết công thức cấu tạo và tên gọi của X. Viết phương trình hoá học của phản ứng điều chế X từ axit và ancol tương ứng.
Phương pháp giải
- Từ sản phẩm cháy ta tìm được số mol C, H và O.
- Tìm công thức đơn giản nhất của X là
- Mà X là este đơn chức, suy ra công thức phân tử của X.
Hướng dẫn giải
Từ sản phẩm cháy ta có :
= nCO2 = 0,2mol → mC = 0,2.12 = 2,4 gam
= 2nH2O = 0,3mol → mH = 0,3.1 = 0,3 gam
= m X − mC −mH = 4,3 − 2,4 − 0,3 = 1,6 gam → nO = 0,1 mol
Đặt công thức phân tử của X là CxHyOz. Ta có tỉ lệ :
x : y : z = 0,2 : 0,3 : 0,1 = 2 : 3 : 1.
CTĐGN của X là C2H3O
Mà X là este đơn chức nên công thức phân tử của X là C4H6O2.
Vì X được tạo ra từ phản ứng este hoá giữa ancol Y và axit hữu cơ Z nên có công thức cấu tạo :
HCOOCH2CH=CH2 (anlyl fomat) hoặc CH2=CHCOOCH3 (metyl acrylat).
OOH + CH2=CH−CH2OH → HCOOCH2−CH=CH2 + H2O
CH2=CH−COOH + CH3OH → CH2=CH−COOCH3 + H2O
13. Giải bài 1.13 trang 5 SBT Hóa học 12
Hỗn hợp X gồm axit axetic và ancol etylic. Chia X thành ba phần bằng nhau. Cho phần một tác dụng với natri dư thấy có 3,36 lít khí H2 thoát ra (đktc). Phần hai phản ứng vừa đủ với 200 ml dung dịch NaOH 1M.
Thêm vào phần ba một lượng H2SO4 làm xúc tác rồi thực hiện phản ứng este hoá, hiệu suất đạt 60%.
a) Viết phương trình hoá học của các phản ứng xảy ra.
b) Tính khối lượng của hỗn hợp X đã dùng và khối lượng este thu được.
Phương pháp giải
Phần 1: nancol + naxit =
Phần 2: naxit = nNaOH
naxit nancol
Phần ba: Vì nancol < naxit hiệu suất tính theo số mol của ancol
neste meste
Hướng dẫn giải
a) Phương trình hoá học của các phản ứng xảy ra:
OOH + Na → CH3COONa + 12H2
C2H5OH + Na → C2H5ONa + 12H2
CH3COOH + NaOH → CH3COONa + H2O
CH3COOH + C2H5OH \(\xrightarrow{{{H_2}S{O_{4(d)}},{t^o}}}\) CH3COOC2H5 + H2O
b)
= 3,36/22,4 = 0,15 mol
nNaOH = 0,2.1 = 0,2 mol
Phần 1: nancol + naxit =
nancol + naxit = 2.0,15
Phần 2: naxit = nNaOH
naxit = 0,2 mol
nancol = 2.0,15 – 0,2 = 0,1 mol
mX = 3.(0,2.60 + 0,1.46) = 49,8 gam.
Phần ba: Vì nancol < naxit hiệu suất tính theo số mol của ancol
= (0,1.60)/100 = 0,06 mol
= mCH3COOC2H5 = 0,06.88 = 5,28 gam
Tham khảo thêm
- doc Giải bài tập SBT Hóa 12 Bài 2: Lipit
- doc Giải bài tập SBT Hóa 12 Bài 3: Khái niệm về xà phòng và chất giặt rửa tổng hợp
- doc Giải bài tập SBT Hóa 12 Bài 4: Luyện tập: Este và chất béo



