Giải bài tập SGK Hóa 12 Bài 10: Amino axit
Nội dung hướng dẫn Giải bài tập Hóa 12 Bài 10 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 48 SGK Hóa 12
Ứng với công thức phân tử C4H9NO2 có bao nhiêu amino axit đồng phân cấu tạo của nhau?
A. 3
B. 4
C. 5
D. 6
Phương pháp giải
Để xác định đồng phân cấu tạo cần nắm các kiến thức sau:
- Amino axit là những hợp chất hữu cơ tạp chức trong phân tử có chứa đồng thời 2 nhóm chức: nhóm amino (NH2) và nhóm cacboxyl (COOH)
- Công thức tổng quát của amino axit là (NH2)x-R-(COOH)y
Hướng dẫn giải
Ứng với công thức phân tử C4H9NO2 ta có các đồng phân sau:
1. CH3-CH2-CH(NH2)-COOH
2. CH3-CH(NH2)-CH2-COOH
3. H2N-CH2-CH2-CH2-COOH
4. H2N-CH2-CH(CH3)-COOH
5. CH3-C(NH2)(CH3)-COOH
→ Đáp án C.
2. Giải bài 2 trang 48 SGK Hóa 12
Có ba chất hữu cơ: H2NCH2COOH, CH3CH2COOH và CH3[CH2]3NH2. Để nhận ra dung dịch của các hợp chất trên, chỉ cẩn dùng thuốc thử nào sau đây?
A. NaOH
B. HCl
C. CH3OH/HCl
D. Quỳ tím
Phương pháp giải
Để nhận biết các dung dịch trên cần nắm các kiến thức sau:
- Amino axit có số nhóm -NH2 bằng với số nhóm -COOH không làm đổi màu quỳ tím
- Amin làm quỳ tím hóa xanh
- Axit cacboxylic làm quỳ tím hóa đỏ (hồng)
Hướng dẫn giải
Cho quỳ tím vào 3 mẫu thử:
- Mẫu thử làm quỳ tím chuyển sang màu đỏ là CH3CH2COOH
- Mẫu thử làm quỳ tím chuyển sang màu xanh là CH3[CH2]3NH2
- Mẫu thử mà quỳ tím không đổi màu là H2NCH2COOH
→ Đáp án D.
3. Giải bài 3 trang 48 SGK Hóa 12
α-Amino axit X có phần trăm khối lượng các nguyên tố C, H, N lần lượt bằng 40,45%, 7,86%, 15,73%, còn lại là oxi và có công thức phân tử trùng với công thức đơn giản nhất. Xác định công thức cấu tạo và gọi tên của X?
Phương pháp giải
Để tìm công thức cấu tạo và gọi tên của X, ta thực hiện các bước:
- Bước 1: Đặt công thức phân tử dạng tổng quát
- Bước 2: Dựa vào phần trăm ta lập tỉ lệ, suy ra x, y, z, t.
- Bước 3: Suy ra công thức phân tử và công thức cấu tạo.
Hướng dẫn giải
Gọi CTPT của X là CxHyOzNt
Ta có
%mO = 100% – (%mC + %mH + %mN) = 100% - (40,45% + 7,86% + 15,73%) = 35,96%
Dựa vào phần trăm các chất ta có tỉ lệ:
\(\begin{array}{l}
\Rightarrow x:y:z:t\\
= \frac{{40,45}}{{12}}:\frac{{7,86}}{1}:\frac{{15,73}}{{14}}:\frac{{35,96}}{{16}}\\
= 3:7:1:2
\end{array}\)
CTĐG của X là C3H7NO2
Vì công thức phân tử của X trùng với công thức đơn giản nhất nên CTPT sẽ là C3H7NO2
CTCT: H2N-CH(CH3)-COOH: alanin.
4. Giải bài 4 trang 48 SGK Hóa 12
Viết phương trình hóa học của các phản ứng giữa axit 2-aminopropanoic với: NaOH; H2SO4; CH3OH có mặt khí HCl bão hòa.
Phương pháp giải
Để viết phương trình hóa học ta cần nắm tính chất hóa học của amino axit.
Hướng dẫn giải
Các phương trình phản ứng như sau:
CH3-CH(NH2)-COOH + NaOH → CH3-CH(NH2)-COONa + H2O
CH3-CH(NH2)-COOH + H2SO4 → CH3-CH(NH3HSO4)-COOH
5. Giải bài 5 trang 48 SGK Hóa 12
Viết phương trình hóa học của phản ứng trùng ngưng các amino axit sau:
a) Axit 7-aminoheptanoic?
b) Axit 10-aminođecanoic?
Phương pháp giải
Để viết phương trình hóa học của phản ứng trùng ngưng các amino axit, ta cần nắm rõ điều kiện và sản phẩm của phản ứng trùng ngưng.
Hướng dẫn giải
Câu a: Phản ứng trùng ngưng axit 7-aminoheptanoic
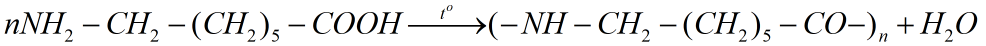
Câu b: Phản ứng trùng ngưng axit 10-aminođecanoic
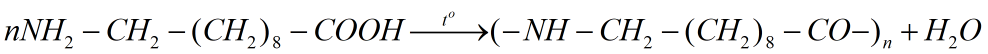
6. Giải bài 6 trang 48 SGK Hóa 12
Este A được điều chế từ amino axit B (chỉ chứa C, H, N, O) và ancol metylic. Tỉ khối hơi của A so với H2 là 44,5. Đốt cháy hoàn toàn 8,9 gam este A thu được 13,2 gam CO2, 6,3 gam H2O và 1,12 lít N2 (đo ở đktc). Xác định công thức, viết công thức cấu tạo của A và B.
Phương pháp giải
Để xác định công thức cấu tạo của A và B, ta thực hiện các bước:
- Bước 1: Bảo toàn nguyên tố: nC=nCO2, nH=2nH2O, nN=2nN2, mO=meste - mC - mH - mN => nO
- Bước 2: Lập tỉ lệ số mol C:H:O:N => CTĐGN
- Bước 3: Suy ra CTPT A(dựa vào tỉ khối của este với H2) và CTCT của A, B.
Hướng dẫn giải
Theo bài ra ta có:
MA = 44,5 . 2 = 89 (g/mol)
\(\begin{array}{l} {n_{C{O_2}}} = \frac{{13,2}}{{44}} = 0,3(mol)\\ {n_{{H_2}O}} = \frac{{6,3}}{{18}} = 0,35(mol)\\ {n_{{N_2}}} = \frac{{1,12}}{{22,4}} = 0,05(mol) \end{array}\)
Áp dụng định luật bảo toàn nguyên tố C, H, N ta có:
\(\begin{array}{l} {n_C} = {n_{C{O_2}}} = 0,3(mol)\\ {n_H} = 2{n_{{H_2}O}} = 2.0,35 = 0,7(mol)\\ {n_N} = 2{n_{{N_2}}} = 2.0,05 = 0,1(mol) \end{array}\)
Ta lại có:
mO = meste - mC - mH - mN = 8,9 - 0,3.12 - 0,7.1 - 0,1.14 = 3,2 gam
Suy ra nO = 3,2 : 16 = 0,2 mol
Gọi CTPT của A là CxHyOzNt
Ta có tỉ lệ:
C : H : O : N = x : y : z : t = 0,3 : 0,7 : 0,1 : 0,1 = 3 : 7 : 2 : 1
⇒ CTĐGN của A là (C3H7O2N)n
Mà MA = 89 g/mol ⇒ n = 1
Vậy CTPT của A là C3H7O2N
Vì A là este của ancol metylic nên CTCT của A là
H2N-CH2-COO-CH3 (A) và H2N-CH2-COOH (B)
Vậy A là C3H7O2N và có 2 công thức cấu tạo như sau: H2N-CH2-COO-CH3 (A) và H2N-CH2-COOH (B).




