Giải bài tập SGK Hóa 12 Nâng cao Bài 11: Amin
Hướng dẫn Giải bài tập Hóa học 12 nâng cao Bài 11 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về tính chất của amin. Mời các em cùng theo dõi.
Mục lục nội dung
1. Giải bài 1 trang 61 SGK Hóa 12 nâng cao
2. Giải bài 2 trang 61 SGK Hóa 12 nâng cao
3. Giải bài 3 trang 61 SGK Hóa 12 nâng cao
4. Giải bài 4 trang 62 SGK Hóa 12 nâng cao
5. Giải bài 5 trang 62 SGK Hóa 12 nâng cao
6. Giải bài 6 trang 62 SGK Hóa 12 nâng cao

1. Giải bài 1 trang 61 SGK Hóa 12 nâng cao
Sự sắp xếp nào theo trật tự tăng dần tính bazơ của các hợp chất sau đây đúng:
A. C2H5NH2 < (C2H5)2NH < NH3 < C6H5NH2
B. (C2H5)2NH < NH3 < C6H5NH2 < C2H5NH2
C. C6H5NH2 < NH3 < C2H5NH2 < (C2H5)2NH
D. NH3 < C2H5NH2 < (C2H5)2NH < C6H5NH2
Phương pháp giải
Để lựa chọn đáp án phù hợp cần ghi nhớ thứ tự tăng dần tính bazơ của các amin.
Hướng dẫn giải
Sự sắp xếp theo trật tự tăng dần tính bazơ là:
C6H5NH2 < NH3 < C2H5NH2 < (C2H5)2NH
⇒ Đáp án C.
2. Giải bài 2 trang 61 SGK Hóa 12 nâng cao
Đốt cháy hoàn toàn 5,9 gam một hợp chất hữu cơ đơn chức X thu được 6,72 lít CO2, 1,12 lit N2 (đktc) và 8,1 gam nước. Công thức của X là:
A. C3H6O
B. C3H5NO3
C. C3H9N
D. C3H7NO2
Phương pháp giải
- Bước 1: Tính số mol nguyên tử C, H và N
- Bước 2: Tính phân tử khối
- Bước 3: Lập tỉ lệ, suy ra công thức cần tìm.
Hướng dẫn giải
Ta có:
\({n_C} = \frac{{6,72}}{{22,4}} = 0,3\;(mol)\)
\(\;{n_H} = \frac{{8,1}}{{18}} . 2 = 0,9\;(mol)\)
Số mol nguyên tử nitơ:
\({n_N} = \frac{{1,12}}{{22,4}}.2 = 0,1\;(mol)\) = nX (X là hợp chất đơn chức)
⇒ Phân tử khối của hợp chất M = \(= \frac{5,9}{0,1} = 59\)
Công thức phân tử C3H9N
⇒ Đáp án C.
3. Giải bài 3 trang 61 SGK Hóa 12 nâng cao
Khái niệm “bậc” của amin khác với khái niệm “bậc“ của ancol và dẫn xuất halogen như thế nào? Viết công thức cấu tạo và gọi tên các đồng phân , chỉ rõ bậc của các amin có cùng công thức phân tử sau:
a) C3H9N.
b) C5H13N.
c) C7H9N (amin thơm).
Phương pháp giải
Để trả lời câu hỏi trên cần nắm rõ lý thuyết về “bậc” của amin khác với khái niệm “bậc“ của ancol và dẫn xuất halogen. Đồng thời nắm rõ cách viết công thức cấu tạo và gọi tên từ công thức phân tử.
Hướng dẫn giải
Sự khác nhau giữa “ bậc” của amin khác với khái niệm “ bậc “ của ancol và dẫn xuất halogen:
Bậc của ancol và dẫn xuất halogen được tính bằng bậc của C mang nhóm chức. Còn bậc của amin được tính bằng số nguyên tử H của amoniac được thay thế bằng gốc hiđrocacbon.
Câu a: Công thức cấu tạo và gọi ten các đồng phân của C3H9N
CH3-CH2-CH2-NH2: n-propyl amin (bậc 1).
CH3-CH(CH3)-NH2 : Iso propyamin (bậc 1).
CH3-NH-CH2-CH3: etyl metyl amin (bậc 2).
CH3-N(CH3)-CH3: trimetyl amin (bậc 3).
Câu b: Công thức cấu tạo và gọi tên các đồng phân C5H13N
Có 16 đồng phân gồm :
- Có 7 amin bậc một:
CH3-CH2-CH2-CH2-CH2-NH2
CH3-CH(NH2)-CH2-CH2-CH3
CH3-CH2-CH(NH2)-CH2-CH3
CH3-CH2-CH(CH3)-CH2-NH2
CH3-CH2-C(NH2)(CH3)-CH3
CH3-CH(CH3)-CH(NH2)-CH3
CH3-CH(CH3)2-CH-NH2
- Có 6 amin bậc hai:
CH3-NH-CH2-CH2-CH2-CH3
CH3-NH-CH2-CH(CH3)-CH3
CH3-NH-CH(CH3)-CH2-CH3
CH3-NH-C(CH3)2-CH3
CH3-CH2-NH-CH2-CH2-CH3
CH3-CH2-NH-CH(CH3)-CH3
- Có 3 amin bậc ba:
CH3-N(CH3)-CH2-CH2-CH3
CH3-CH2-N(CH3)-CH2-CH3
CH3-N(CH3)-CH(CH3)-CH3
Câu c: Công thức cấu tạo và gọi tên các đồng phân C7H9N (có chứa vòng benzen)

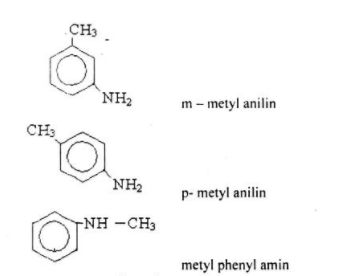
4. Giải bài 4 trang 62 SGK Hóa 12 nâng cao
a) Vì sao amin dễ tan trong nước hơn so với dẫn xuất halogen có cùng số nguyên tử C trong phân tử?
b) Vì sao benzylamin (C6H5CH2NH2) tan vô hạn trong nước và làm xanh quỳ tím còn anilin thì tan kém (3,4 gam trong 100 g nước) và không làm đổi màu quỳ tím?
Phương pháp giải
Để trả lời câu hỏi trên cần nắm rõ lý thuyết về bản chất và đặc điểm cấu tạo của amin.
Hướng dẫn giải
Câu a
Amin dễ tan trong nước hơn so với dẫn xuất halogen có cùng số nguyên tử C trong phân tử vì giữa phân tử amin và phân tử nước có liên kết hiđro do đó amin dễ tan trong nước hơn dẫn xuất halogen.
Câu b
- Đôi electron trên nguyên tử trên nitơ của phân tử anilin tạo ra được hiệu ứng liên hợp p−π với vòng benzen; còn đôi electron trên nguyên tử nitơ của phân tử C6H5CH2NH2 thì không tạo ra được ⇒ Mật độ của electron trên nguyên tử nitơ của phân tử anilin kém hơn so với C6H5CH2NH2
- C6H5CH2NH2 tan vô hạn trong nước còn anilin thì tan kém là do C6H5CH2NH2 tạo liên kết hidro với nước giúp nó phân tán tốt trong nước.
- C6H5CH2NH2 làm quỳ tím hóa xanh còn anilin thì không làm đổi màu quỳ tím là do tính bazơ của C6H5CH2NH2 mạnh hơn tính bazơ của anilin.
5. Giải bài 5 trang 62 SGK Hóa 12 nâng cao
Trình bày cách để tách riêng mỗi chất ra khỏi hỗn hợp sau đây:
a. Hỗn hợp khí: CH4 và CH3NH2
b. Hỗn hợp lỏng: C6H6, C6H5OH, C6H5NH2
Phương pháp giải
Để tách riêng mối chất ra khỏi hỗn hợp cần nắm rõ tính chất đặc trưng và khác biệt để lựa chựa hóa chất và phương pháp phù hợp.
Hướng dẫn giải
Câu a: Tách hỗn hợp khí CH4 và CH3NH2
- Cho hỗn hợp đi qua dung dịch HCl ta được CH3NH2 phản ứng với HCl bị giữ lại trong dung dịch, khí thoát ra ngoài là CH4 tinh khiết.
CH3NH2 + HCl → CH3NH2Cl
- Cho NaOH vào CH3NH2Cl thu lại được CH3NH2.
CH3NH2Cl + NaOH → CH3NH2 + NaCl + H2O
Câu b: Tách riền hỗn hợp lỏng: C6H6, C6H5OH, C6H5NH2
- Hòa tan hỗn hợp vào dung dịch HCl, chiết lấy phần lỏng không tan là C6H6 và C6H5OH còn C6H5NH2 tan và tạo muối
C6H5NH2 + HCl → C6H5NH3Cl
- Dung dịch muối thu được cho tác dụng với NaOH, chiết lấy anilin
C6H5NH3Cl + NaOH → C6H5NH2 + H2O + NaCl
- Phần không tan trong dung dịch HCl là benzen và phenol đem hòa tan trong dung dịch NaOH, chiết lấy chất lỏng không tan là C6H6 còn phenol tan và tạo muối:
C6H5OH + NaOH → C6H5ONa + H2O
- Sục khí CO2 vào dung dịch muối rồi chiết lấy phenol không tan
C6H5ONa + CO2 + H2O → C6H5OH + NaHCO3
6. Giải bài 6 trang 62 SGK Hóa 12 nâng cao
Trình bày phương pháp hóa học để phân biệt các dung dịch của các chất trong từng dãy sau:
a. C2H5NH2, C6H5NH2, CH2O[CHOH]4CHO, CH2OH-CHOH-CH2OH.
b. CH3NH2, C6H5OH, CH3COOH, CH3CHO.
Phương pháp giải
Để phân biệt các dung dịch cần nắm rõ tính chất đặc trưng và khác biệt để lựa chựa hóa chất và phương pháp phù hợp.
Hướng dẫn giải
Câu a
- Dùng quỳ tím nhận biết được C2H5NH2 vì C2H5NH2 làm quỳ tím hóa xanh.
- Dùng Cu(OH)2 ở nhiệt độ thường, C6H5NH2 không hiện tượng.
CH2OH[CHOH]4CHO,CH2OHCHOHCH2OH tạo ra dung dịch xanh lam trong suốt:
2C6H12O6 + Cu(OH)2 →(C6H11O6)2Cu+H2O
2C3H8O3 + Cu(OH)2→(C3H7O3)2Cu+2H2O
- Dùng Cu(OH)2 đun nóng nhận biết được CH2OH[CHOH]4CHO vì tạo ra kết tủa đỏ gạch:
HOCH2(CHOH)4CHO + 2Cu(OH)2 + NaOH \(\xrightarrow{{{t^o}}}\) CH2OH(CHOH)4COONa + Cu2O↓ + 3H2O
Câu b
Dùng quỳ tím nhận biết được CH3NH2,CH3COOH vì CH3NH2 làm quỳ tím hóa xanh; CH3COOH làm quỳ tím hóa đỏ.
Dùng phản ứng tráng gương nhận biết được CH3CHO vì tạo ra kết tủa Ag.
CH3CHO + 2[Ag(NH3)2]OH \(\xrightarrow{{N{H_3},{t^o}}}\) CH3COONH4 + 2Ag + 3NH3 + H2O
7. Giải bài 7 trang 62 SGK Hóa 12 nâng cao
Hãy dùng phương pháp học để giải quyết hai vấn đề sau:
a. Rửa lọ đựng anilin.
b. Khử mùi tanh của cá trước khi nấu. Biết rằng mùi tanh của cá (đặc biệt cá mè) là hỗn hợp cac amin (nhiều chất là trimetylamin) và một số tạp chất khác.
Phương pháp giải
Để xác định phương pháp phù hợp giải quyết các vấn đề trên cần nắm rõ tính chất hóa học của các chất đó.
Hướng dẫn giải
Câu a: Rửa lọ đựng anilin
Để rửa lọ đựng anilin trước tiên ta tráng lọ bằng dung dịch axit (ví dụ: HCl) rồi rửa lại bằng nước khi đó anilin biến thành muối tan (C6H5NH3Cl) và sẽ bị rửa trôi theo nước.
Câu b: Khử mùi tanh của cá trước khi nấu
Để khử mùi tanh của cá do các amin gây ra cần xử lí bằng dung dịch có tính axit không độc như giấm ăn rồi rửa lại với nước sạch.
8. Giải bài 8 trang 62 SGK Hóa 12 nâng cao
Khi chưng cất nhựa than đá, người ta thu được một phân đoạn chứa phenol và anilin hòa tan trong ankylbenzen (dung dịch A). Sục khí hiđro clorua vào 100 ml dung dịch A thì thu được 1,295 gam kết tủa. Nhỏ từ từ nước brom vào 100ml dung dịch A và lắc kĩ cho đến khi ngừng tạo kết tủa trắng thì hết 300 gam nước brom 3,2%. Tính nồng độ mol của anilin và phenol trong dung dịch A.
Phương pháp giải
- Bước 1: Gọi số mol của C6H5OH, C6H5NH2 lần lượt là x, y; viết phương trình hóa học
- Bước 2: Từ số mol kết tủa, suy ra mol HCl, brom
- Bước 3: Dựa vào phương trình, suy ra mol C6H5OH, C6H5NH2.
→ nồng độ mol của anilin và phenol
Hướng dẫn giải
Gọi số mol của C6H5OH, C6H5NH2 lần lượt là x, y (trong 100 ml dung dịch A)
A + HCl:
C6H5NH2 + HCl → C6H5NH3Cl (1)
Theo (1) nHCl phản ứng = nanilin = nmuối = \(\frac{1,295}{129,5} = 0,01 \ (mol)\)
A + dd Br2:
C6H5OH + 3Br2 → C6H2Br3OH + 3HBr (2)
z mol 3z mol z mol
C6H5OH + 3Br2 → C6H2Br3NH2 + 3HBr (3)
0,01 mol 0,03 mol 0,01 mol
Coi dung dịch loãng của nước brom có d = 1 g/ml, theo đề bài ta có:
\(n_{Br_{2}} = \frac{300 . 3,2 \%}{160} = 0,06 \ (mol)\)
⇒ 3z = 0,06 - 0,03 mol hay z = 0,01 mol
\(C_{M \ anilin} = C_{M \ phenol} = \frac{0,01}{0,1} = 0,1 \ M\)
Tham khảo thêm
- doc Giải bài tập SGK Hóa 12 Nâng cao Bài 12: Amino axit
- doc Giải bài tập SGK Hóa 12 Nâng cao Bài 13: Peptit và protein
- doc Giải bài tập SGK Hóa 12 Nâng cao Bài 14: Luyện tập: Cấu tạo và tính chất của amin, amino axxit, protein



