Giải bài tập SGK Hóa 12 Bài 23: Luyện tập: Điều chế kim loại và sự ăn mòn kim loại
Nội dung hướng dẫn Giải bài tập Hóa 12 Bài 23 dưới đây sẽ giúp các em học sinh nắm vững phương pháp giải bài tập và ôn luyện tốt kiến thức về điều chế kim loại và sự ăn mòn kim loại. Mời các em cùng theo dõi.
Mục lục nội dung

1. Giải bài 1 trang 103 SGK Hóa học 12
Bằng phương pháp nào có thể điều chế được Ag từ dung dịch AgNO3, điều chế Mg từ dung dịch MgCl2? Viết các phương trình hoá học.
Phương pháp giải
Để điều chế các kim loại trên cần ghi nhớ
+ Cách điều chế kim loại Ag: phương pháp thủy luyện, phương pháp nhiệt luyện, phương pháp điện phân dung dịch
+ Cách điều chế kim loại Mg: điện phân nóng chảy muối clorua
=> Viết được PTHH xảy ra.
Hướng dẫn giải
- Từ dung dịch AgNO3 có 3 cách để điều chế Ag:
- Phương pháp thủy luyện: dùng kim loại có tính khử mạnh hơn để khử ion Ag+.
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
- Phương pháp điện phân dung dịch AgNO3:
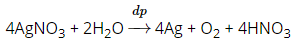
- Cô cạn dung dịch rồi nhiệt phân AgNO3:
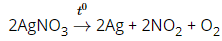
- Từ dung dịch MgCl2 điều chế Mg: chỉ có một cách là cô cạn dung dịch để lấy MgCl2 khan rồi điện phân nóng chảy:
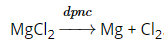
2. Giải bài 2 trang 103 SGK Hóa học 12
Ngâm một vật bằng đồng có khối lượng 10 gam trong 250 gam dung dịch AgNO3 4%. Khi lấy vật ra thì khối lượng AgNO3 trong dung dịch giảm 17%.
a) Viết phương trình hoá học của phản ứng và cho biết vai trò các chất tham gia phản ứng.
b) Xác định khối lượng của vật sau phản ứng.
Phương pháp giải
Để trả lời các câu hỏi trên ta cần lưu ý:
a) Viết PTHH: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
Xác định chất nào có số oxi hóa tăng sau phản ứng thì chất đó đóng vai trò là chất khử
Chất nào có số oxi hóa giảm sau phản ứng chất đó đóng vai trò là chất oxi hóa
b)Tính nAgNO3 phản ứng
Dựa vào PTHH, tính được mol Cu phản ứng và Ag tạo thành theo số mol của nAgNO3
=> m sau = mCu dư + mAg
Hướng dẫn giải
Câu a: Phương trình hoá học của phản ứng
2AgNO3 + Cu → Cu(NO3)2 + 2Ag
Phương trình ion thu gọn: Cu + 2Ag+ → Cu2+ + 2Ag↓
Cu đóng vai trò là chất khử (vì số oxi hóa tăng sau pư)
AgNO3 đóng vai trò là chất oxi hóa (vì số oxi hóa giảm sau phản ứng)
Câu b: Khối lượng của vật sau phản ứng
\({{m_{AgN{O_3}}} = \frac{{250,4}}{{100}} = 10\;(gam)}\)
\({ \Rightarrow {n_{AgN{O_{{3_{}}}}}} = \frac{{10}}{{170}} = 1/17\;mol}\)
Vì khối lượng AgNO3 trong dung dịch giảm 17% nên lượng AgNO3 phản ứng bằng 17% lượng AgNO3 ban đầu
→ \({n_{AgN{O_3}\,(pu)}} = \frac{1}{{17}}.\frac{{17}}{{100}} = 0,01\) mol
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag
0,005 0,01 0,01
Khối lượng của vật sau phản ứng là:
m sau = m Cu dư + mAg = (10 – 64.0,005) + 108.0,01 = 10,76 (gam)
3. Giải bài 3 trang 103 SGK Hóa học 12
Để khử hoàn toàn 23,2 gam một oxit kim loại, cần dùng 8,96 lít H2 (đktc). Kim loại đó là:
A. Mg.
B. Cu.
C. Fe.
D. Cr.
Phương pháp giải
Để xác định kim loại ta thực hiện các bước:
- Bước 1; Gọi CTTQ của oxit kim loại là MxOy
- Bước 2: PTHH: MxOy + yH2 → xM + yH2O
- Bước 3: nMxOy = 1/ynH2=0,4/y(mol)
=>MMxOy= moxit/noxit=23,2:(0,4/y) = 58y =>Mx + 16y = 58y =>Mx=42y
- Bước 4: Biện luận tìm x,y, M
Hướng dẫn giải
Gọi CTTQ của oxit kim loại là MxOy
Ta có phương trình hóa học như sau:
MxOy + yH2 → xM + yH2O (1)
Ta có: \({n_{{H_2}}} = \frac{{8,96}}{{22,4}} = 0,4{\mkern 1mu} mol\)
Theo (1) ta lại có:
\(\begin{array}{*{20}{l}} {{n_{{M_x}{O_y}}} = \frac{1}{y}.{n_{{H_2}}} = \frac{{0,4}}{y}{\mkern 1mu} mol}\\ { \to {M_{{M_x}{O_y}}} = \frac{{{m_{oxit}}}}{{{n_{oxit}}}} = \frac{{23,2}}{{\frac{{0,4}}{y}}} = 58y} \end{array}\)
→ Mx + 16y = 58y
→ Mx = 42y
Biện luận tìm x, y và M
Với M = 56, x = 3 và y = 4 (thỏa mãn)
Vậy kim loại cần tìm là Fe.
→ Chọn C.
4. Giải bài 4 trang 103 SGK Hóa học 12
Cho 9,6 gam bột kim loại M vào 500 ml dung dịch HCl 1M, khi phản ứng kết thúc thu được 5,376 lít H2 (đktc). Kim loại M là:
A. Mg.
B. Ca.
C. Fe.
D. Ba.
Phương pháp giải
Để xác định kim loại M ta thực hiện các bước:
- Bước 1: Gọi hóa trị của kim loại là n
- Bước 2: Viết PTHH xảy ra, tính số mol của kim loại M theo số mol của H2
2M + 2nHCl → 2MCln + nH2
- Bước 3: Biện luận tìm M.
Hướng dẫn giải
Gọi hoá trị của kim loại M là n:
2M + 2nHCl → 2MCln + nH2 (1)
\(\\ n_{H_{2}} = \frac{5,376}{22,4} = 0,24\)
Ta thấy nHCl = 0,5 > 2nH2 = 0,48 ⇒ HCl dư, kim loại phản ứng hết
Từ (1) \(\Rightarrow n_{M} = \frac{0,24.2}{n} = \frac{0,48}{n} \ (mol)\)
Ta có:
\(\frac{0,48}{n} .M = 96 \Rightarrow M = \frac{9,6n}{0,48}\)
Biên luận:
n = 1 → M = 20 (loại)
n = 2 → M = 40 (Ca)
n = 3 → M = 60 (loại)
Vậy kim loại cần tìm là Ca → Đáp án B.
5. Giải bài 5 trang 103 SGK Hóa học 12
Điện phân nóng chảy muối clorua M. Ở catot thu được 6 gam kim loại và ở anot có 3,36 lít khí (đktc) thoát ra. Muối clorua đó là:
A. NaCl.
B. KCl.
C. BaCl2.
D. CaCl2.
Phương pháp giải
Để xác định muối clorua ta thực hiện các bước:
- Bước 1: Viết phương trình hóa học:
2MCln \(\xrightarrow{{dpnc}}\) 2M + nCl2
Tính nCl2 => nM = ?
- Bước 2: Ta có: MM = m : nM => tìm được mối quan hệ giữa M và n.
- Bước 3: Biên luận tìm được M.
Hướng dẫn giải
Phương trình hóa học của phản ứng như sau:
2MCln → 2M + nCl2
Dựa vào PTHH và đề bài ta có:
\(\begin{array}{l}
{n_{C{l_2}}} = \frac{{3,36}}{{22,4}} = 0,15\;mol\\
\Rightarrow {n_M} = \frac{{0,15.2}}{n} = \frac{{0,3}}{n}\;(mol)
\end{array}\)
Ta có:
\(\frac{0,3}{n.M} = 6\)
Chỉ có n = 2 và M = 40 là phù hợp
⇒ M là Ca
Vậy muối đó là CaCl2.
⇒ Chọn D.
Tham khảo thêm
- doc Giải bài tập SGK Hóa 12 Bài 17: Vị trí của KL trong bảng tuần hoàn và cấu tạo của KL
- doc Giải bài tập SGK Hóa 12 Bài 18: Tính chất của kim loại. Dãy điện hóa của kim loại
- doc Giải bài tập SGK Hóa 12 Bài 19: Hợp kim
- doc Giải bài tập SGK Hóa 12 Bài 20: Sự ăn mòn kim loại
- doc Giải bài tập SGK Hóa 12 Bài 21: Điều chế kim loại
- doc Giải bài tập SGK Hóa 12 Bài 22: Luyện tập tính chất của kim loại



