Giải bài tập SGK Hóa 11 Bài 37: Nguồn hiđrocacbon thiên nhiên
eLib xin giới thiệu đến quý thầy cô giáo và các em học sinh nội dung giải bài tập Nguồn hiđrocacbon thiên nhiên SGK Hóa học 11 dưới đây. Tài liệu gồm các bài tập có phương pháp và hướng dẫn giải chi tiết sẽ giúp các em ôn tập thật tốt kiến thức, cũng cố kỹ năng làm bài tập hiệu quả. Mời các em cùng tham khảo.
Mục lục nội dung

1. Giải bài 1 trang 169 SGK Hóa học 11
Hãy cho biết thành phần dầu mỏ. Tại sao dầu mỏ không có nhiệt độ sôi nhất định? có thể biểu thị thành phần của dầu mỏ bằng một công thức phân tử nhất định được không? Tại sao?
Phương pháp giải
Xem lại lý thuyết về nguồn hidrocacbon thiên nhiên
Hướng dẫn giải
- Thành phần dầu mỏ: là hỗn hợp của rất nhiều các hiđrocacbon khác nhau, thành phần cơ bản gồm các loại ankan, xicloankan, aren ngoài ra còn 1 só lượng nhỏ các chất hữu cơ chứa oxi, nito, lưu huỳnh và vết các chất hữu cơ.
- Lý do dầu mỏ không có nhiệt độ sôi nhất định vì
Một cách chính xác thì dầu mỏ là hỗn hợp của các hiđrocacbon, là hợp chất của hiđro và cacbon. Nên nó không có nhiệt độ sôi nhất định.
Trong điều kiện thông thường, bốn ankan nhẹ nhất - CH4 (metan), C2H6 (etan), C3H8 (propan) và C4H10 (butan) - ở dạng khí, sôi ở nhiệt độ - 161.6 °C, - 88.6 °C, - 42 °C, và - 0.5 °C tương ứng (- 258.9°, --127.5°, --43.6°, và --31.1 °F).
- Dầu mỏ không có công thức nhất định cũng vì lý do trên.
Thành phần chính của dầu mỏ là metan , etan , butan , và propan .Còn có rất nhiều các chất khác nhưng tỷ lệ 4 chất này là nhiều nhất.
2. Giải bài 2 trang 169 SGK Hóa học 11
Khí thiên nhiên, khí dầu mỏ, khí lò cốc là gì? Nêu thành phần chính của mỗi loại khí này và ứng dụng của nó.
Phương pháp giải
Xem lại lý thuyết về nguồn hidrocacbon thiên nhiên
Hướng dẫn giải
- Khí thiên nhiên có trong các mỏ khí riêng biệt, khí dầu mỏ có trong các mỏ dầu.
- Thành phần gồm: metan (trong khí thiên nhiên metan chiếm từ 75-95%), etan, propan, butan, pentan và một số khí vô cơ khác ( như nito, hidro,hidrosunfua,...)
- Khí lò cốc: là hỗn hợp các chất dễ cháy. thành phần phụ thuộc vào nguyên liệu ban đầu nhưng hàm lượng trung bình các chất theo thành phần phần trăm thể tích.( tham khảo sgk trang 168)
- Ứng dụng:làm nhiên liệu cho các nhà mấy nhiệt điện.
3. Giải bài 3 trang 169 SGK Hóa học 11
Trình bày tóm tắt quy trình chưng cất dầu mỏ, các phân đoạn và ứng dụng của chúng. Có mấy loại than chính? Thành phần và cách chế biến chúng.
Phương pháp giải
Xem lại lý thuyết về nguồn hidrocacbon thiên nhiên, quy trình sản xuất dầu mỏ, các sơ đồ điều chế, chưng cất...
Hướng dẫn giải
Sơ đồ quy trình chưng cất dầu mỏ:
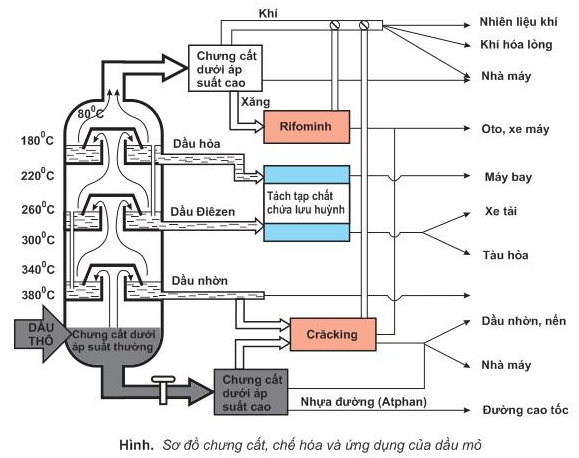
- Phân đoạn và ứng dụng:
+ Dầu khai thác từ mỏ lên gọi là dầu thô. Dầu thô sau khi sơ chế loại bỏ nước, muối, được chưng cất ở áp suất thường trong các tháp chưng cất phân đoạn liên tục cao vài chục mét. Nhờ vậy người ta tách được những phân đoạn dầu có nhiệt độ sôi khác nhau. Các phân đoạn đó được đưa đi sử dụng hoặc được chế biến tiếp.
+ Các sản phẩm chưng cất dầu mỏ ở áp suất thường:
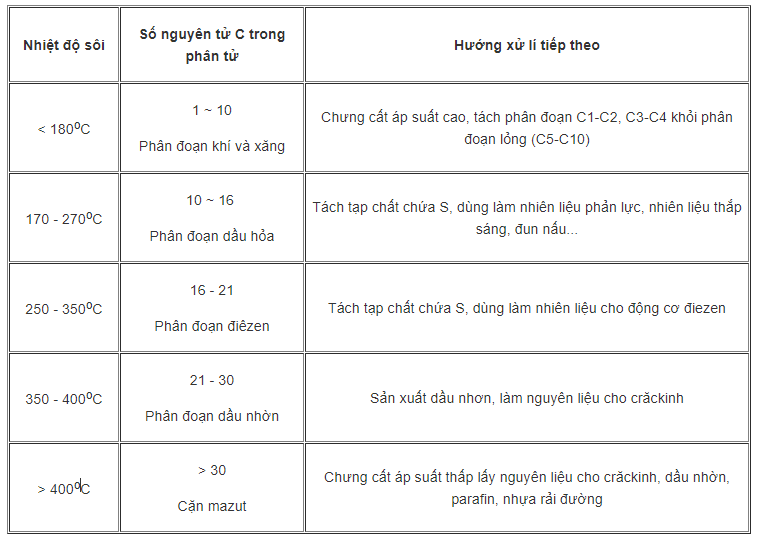
Trong các loại than mỏ (than gầy, than béo, than bùn,…) hiện nay chỉ có than béo (than mỡ) được dùng để chế biến than cốc và cung cấp một lượng nhỏ hiđrocacbon. Than gầy chủ yếu dùng làm nhiên liệu cho các nhà máy nhiệt điện, xi măng, vv…
4. Giải bài 4 trang 169 SGK Hóa học 11
Một loại khí thiên nhiên có thành phần phần trăm về thể tích các khí như sau: 85% metan; 10,0% etan; 2,0% nitơ và 3,0% cacbon đioxit.
a) Tính thể tích khí (đo ở điều kiện tiêu chuẩn) cần để đun nóng 100,0 lít nước từ 20,0oC lên 100oC, biết nhiệt lượng tỏa ra khi đốt 1 mol metan, 1 mol etan lần lượt bằng: 880,0 kJ; 1560,0 kJ và để nâng 1 ml nước lên 10 cần 4,18 J.
b) Nếu chuyển được toàn bộ hiđrocacbon trong 1,000.103 m3 khí trên (đktc) thành axetilen, sau đó thành vinyl clorua với hiệu suất toàn bộ quá trình bằng 65,0% thì sẽ thu được bao nhiêu kilogram vinyl clorua?
Phương pháp giải
a) Nhiệt lượng cần để để đun nóng 100 lít nước từ 20oC lên 100oC
[4,18x(100 – 20).105 = 334.105 (J) = 334.102 KJ.
Gọi số mol khí thiên nhiên là x mol.
Vậy: số mol CH4 là 0,85x mol; số mol C2H6 là 0,1x mol.
Do đó: 0,85x mol CH4 tỏa ra nhiệt lượng là: 880 x 0,85x = 748 (kJ).
0,1x mol C2H6 tỏa ra nhiệt lượng là 1560 x 0,10x = 156x (kJ).
Ta có: 748x + 156x = 334x102 → x = ? mol.
b) Viết PTHH xảy ra, tính toán theo PTHH
\(\% H = \frac{{Luong{\mkern 1mu} thuc{\mkern 1mu} te}}{{Luong{\mkern 1mu} li{\mkern 1mu} thuyet}}.100\% \)
Hướng dẫn giải
a) Nhiệt lượng cần để để đun nóng 100 lít nước từ 20oC lên 100oC
[4,18x(100 – 20).105 = 334.105 (J) = 334.102 KJ.
Gọi số mol khí thiên nhiên là x mol.
Vậy: số mol CH4 là 0,85x mol; số mol C2H6 là 0,1x mol.
Do đó: 0,85x mol CH4 tỏa ra nhiệt lượng là: 880 x 0,85x = 748x (kJ).
0,1x mol C2H6 tỏa ra nhiệt lượng là 1560 x 0,10x = 156x (kJ).
Ta có: 748x + 156x = 334x102 => x = 36,9 mol.
Vậy, thể tích khí thiên nhiên cần dùng để đun nóng 100 lít nước từ 20oC lên 100oC là 22,4x = 827 lít.
b) 827 lít khí thiên nhiên có 0,85x mol CH4 và 0,1x mol C2H6
106 lít khí thiên nhiên có a mol CH4 và b mol C2H6.
a = \(\dfrac{10^{6}x0,85x36,9}{827}\) = 3,79.104 (mol) CH4
b = \(\dfrac{10^{6}x0,1x36,991}{827}\) = 4,46.103 (mol) C2H6.
2C2H4 → C2H2 → C2H3Cl
2 mol 1mol
3,79.104 mol 1,9.104 mol
C2H6 → C2H2 → C2H3Cl
1 mol 1 mol
4,46.103 mol 4,46.103 mol
Số mol C2H3Cl thực tế thu được:
(1,9.104 + 4,46.103).0,65 = 1,52.104 (mol)
Khối lượng C2H3Cl thực tế thu được:
1,52.104.62,5 = 95.104 (g) = 950 kg.
Tham khảo thêm
- doc Giải bài tập SGK Hóa 11 Bài 35: Benzen và đồng đẳng. Một số hiđrocacbon thơm khác
- doc Giải bài tập SGK Hóa 11 Bài 36: Luyện tập Hiđrocacbon thơm
- doc Giải bài tập SGK Hóa 11 Bài 38: Hệ thống hóa về hiđrocacbon



